Babesiose des Hundes
Die Babesiose des Hundes (Syn. „Hundemalaria“, Piroplasmose) ist eine durch Einzeller der Gattung Babesia hervorgerufene Infektionskrankheit bei Hunden, die eine Zerstörung der roten Blutkörperchen und damit eine mehr oder weniger ausgeprägte Blutarmut (Anämie) hervorruft.
Die Erkrankung verläuft in Deutschland meistens akut mit hohem Fieber und endet ohne Behandlung binnen weniger Tage tödlich. Die Übertragung erfolgt durch Zecken. Während die Babesiose bis in die 1970er Jahre vor allem eine „Reisekrankheit“ war, kommt sie durch die Ausdehnung des Verbreitungsgebiets der Auwaldzecke mittlerweile natürlich in Deutschland vor. Die Diagnose wird über einen Nachweis der Babesien-DNA oder eine mikroskopische Untersuchung des Blutes gesichert. Zur Behandlung werden Antiprotozoika eingesetzt.
Andere Tierarten oder der Mensch sind durch die beim Hund krankheitsauslösenden Babesien nicht gefährdet. Allerdings kommen auch bei anderen Säugetieren Erkrankungen durch zumeist wirtsspezifische Babesien vor (→ Babesiose des Menschen und Systematik der Babesien).
Erreger und Verbreitung
Babesien sind Einzeller, die als Parasiten die roten Blutkörperchen befallen. Sie werden den Apicomplexa zugeordnet. Ein Abschnitt ihres Vermehrungszyklus findet im Zwischenwirt – verschiedenen Zeckenarten – statt. Die Babesiose der Hunde wird durch mehrere Babesienarten hervorgerufen, die für andere Tierarten nicht krankheitserregend sind.
Babesia canis ist eine relative große Babesienart (2–4 × 4–7 μm), die weltweit vorkommt. Man unterscheidet heute drei Unterarten, die sich hinsichtlich ihrer DNA und ihres Vektors, aber nicht morphologisch unterscheiden:
- Babesia canis canis wird durch die Auwaldzecke (Dermacentor reticularis) übertragen, die sich mittlerweile in ganz Mitteleuropa ausgebreitet hat.[2] Diese Babesien-Unterart ist im deutschsprachigen Raum am häufigsten für Erkrankungen bei Hunden verantwortlich. Ursprünglich nur in Nordafrika, Nord- und Mittelitalien, Frankreich und im südlichen Teil Ungarns und Österreichs vorkommend, gibt es mittlerweile Naturherde in Deutschland, der Schweiz, Holland und Polen. Der Erreger ist stark krankheitsauslösend.
- Babesia canis vogeli wird durch die Braune Hundezecke (Rhipicephalus sanguineus) übertragen. Infektionen mit diesem Erreger sind in Mitteleuropa selten und verlaufen mild. Verbreitet ist B. c. vogeli in Nordafrika, dem Mittelmeerraum und Frankreich.
- Babesia canis rossi wird durch Haemaphysalis leachi verbreitet und kommt nur in Afrika südlich der Sahara vor. Der Erreger ist stark krankheitsauslösend.
Das ursprüngliche Verbreitungsgebiet der Babesiose (Enzootiegebiet) innerhalb Europas beschränkte sich bis in die 1970er Jahre auf Südeuropa, so dass die Erkrankung in Deutschland nahezu ausschließlich bei Hunden nach Urlaubsreisen in diese Region auftrat.
Mit der Ausbreitung der Auwaldzecke auf ganz Mitteleuropa kommen ortsständige Krankheitsfälle auch in Deutschland vor: Etwa ein Drittel der erkrankten Hunde hatte niemals einen Auslandsaufenthalt. Die Durchseuchung der Auwaldzecken mit Babesien ist in Deutschland zwar noch relativ gering, allerdings stetig ansteigend. Etwa 0,5 % der Auwaldzecken sind Babesienträger.
Nachdem zunächst nur am Oberrhein ortsständige Infektionen beobachtet wurden, gibt es mittlerweile Enzootiegebiete im Saarland, in Rheinland-Pfalz, in den Isarauen bei München, in der Umgebung von Regensburg, in den Elbauen und in Brandenburg. Derzeit werden einige tausend Erkrankungen pro Jahr in Deutschland festgestellt. Davon sind etwa 300–400 ortsständige Infektionen, die fast alle im Saarland und am Oberrhein auftreten.
Krankheitsentstehung
Die Übertragung beim Zeckenstich dauert etwa 48 bis 72 Stunden, unter experimentellen Bedingungen konnte bereits nach 12 Stunden nach Anheften der Zecke eine Übertragung von B. c. canis nachgewiesen werden.
Durch das Anheften der Zecke an den Wirt werden durch Reizung des Nervensystems die in verschiedenen Organen ruhenden Sporozoiten aktiviert und entwickeln sich zu Kineten, die dann in die Speicheldrüsen einwandern und mit dem Zeckenspeichel in den Blutkreislauf des Hundes gelangen.
Neben der Übertragung durch Zecken ist eine Infektion von Hund zu Hund über eine Bluttransfusion oder durch Blut-Blut-Kontakte – beispielsweise bei Beißereien – möglich.
Krankheitsbild
In Deutschland tritt vor allem die akut verlaufende Form der Babesia-canis-canis-Infektion auf. Die Inkubationszeit beträgt 5 bis 7 Tage, selten kann sie bis zu drei Wochen nach dem Zeckenstich dauern.
Krankheitszeichen (Symptome) sind ein gestörtes Allgemeinbefinden und Fieber, gefolgt von Fressunlust, Gewichtsverlust und Abgeschlagenheit. Ein bis zwei Tage später kommt es aufgrund des Zerfalls der roten Blutkörperchen (Hämolyse) zu Blutarmut (Anämie), Blutharnen, Ausscheidung des Blutfarbstoffabbauprodukts Bilirubin über den Harn (Bilirubinurie) und gegebenenfalls auch Gelbsucht. Eine Leber- und Milzvergrößerung kommt häufig vor.
Bei schweren Verläufen treten eine Bauchwassersucht und Wasseransammlungen (Ödeme) sowie Haut- und Schleimhautblutungen infolge Blutplättchenmangel (Thrombozytopenie) und eine Blutgerinnung innerhalb der Blutgefäße (disseminierte intravasale Koagulopathie) auf. Entzündungen der Maul- (Stomatitis) und Magenschleimhaut (Gastritis) sowie der Muskulatur (Myositis) sind häufig. Auch eine zentralnervöse Form mit epilepsieähnlichen Anfällen, Bewegungsstörungen und Lähmungen ist möglich.
Die akute Form endet unbehandelt binnen weniger Tage mit dem Tod durch Atemnot, Anämie und Nierenversagen, welches eine gefürchtete Komplikation einer Babesiose ist. Der seltene perakute Verlauf endet ohne deutliche Symptome binnen ein bis zwei Tagen tödlich.
Diagnostik
Die Babesiose kann klinisch mit einer Vielzahl anderer fieberhafter Erkrankungen verwechselt werden. Die Diagnose ist über einen normalen Blutausstrich („Dünner Tropfen“) oder den so genannten „Dicken Tropfen“ möglich, wobei Kapillarblut sensitiver ist als venöses Blut.
Die Erreger können in der Frühphase der Infektion und in den Phasen zwischen den Vermehrungsschüben im Blut (Parasitämie) nur in geringer Zahl auftreten und damit übersehen werden. Sicher ist der Nachweis im Blutausstrich erst etwa 7 Tage nach der Infektion. Die Babesien können unter dem Mikroskop nachgewiesen werden, wobei die Giemsa-Färbung – im Gegensatz zu den üblichen Schnellfärbungen – am zuverlässigsten ist
Behandlung und Vorbeugung
Da die Krankheit ohne Behandlung schnell tödlich endet, sollte bei Verdacht unverzüglich eine Therapie eingeleitet werden. Antiprotozoika wie Imidocarb oder Diminazen sind gegen B. canis gut, gegen „kleine Babesien“ dagegen nur wenig wirksam. Imidocarb kann auch zur Prophylaxe bei Reisen in Endemiegebiete einmalig verabreicht werden – der Schutz hält etwa drei Wochen an. Eine Kombination aus Atovaquon und Azithromycin kann auch chronische Infektionen mit B. gibsoni heilen. Auch Phenamidin ist gegen „kleine Babesien“ wirksam, aber derzeit in Deutschland nicht erhältlich. In akuten Fällen ist bei einem Hämatokrit unter 20 eine Bluttransfusion oder die Gabe von Hämoglobin-Glutamer 200 angezeigt.
Die wichtigste Prophylaxe ist das Absuchen des Tieres nach Zecken nach jedem Spaziergang und deren sofortige Entfernung. Ein Schutz vor Zecken durch äußerlich anzuwendende zeckenabtötende Wirkstoffe (Akarizide wie Amitraz, Deltamethrin, Fipronil, Flumethrin oder Permethrin) ist sinnvoll, da sie auch die Gefahr des Auftretens weiterer, durch Zecken auf Hunde übertragbarer Erkrankungen wie Borreliose, Ehrlichiose, Hepatozoonose oder FSME senken.
Die Erkrankung verläuft in Deutschland meistens akut mit hohem Fieber und endet ohne Behandlung binnen weniger Tage tödlich. Die Übertragung erfolgt durch Zecken. Während die Babesiose bis in die 1970er Jahre vor allem eine „Reisekrankheit“ war, kommt sie durch die Ausdehnung des Verbreitungsgebiets der Auwaldzecke mittlerweile natürlich in Deutschland vor. Die Diagnose wird über einen Nachweis der Babesien-DNA oder eine mikroskopische Untersuchung des Blutes gesichert. Zur Behandlung werden Antiprotozoika eingesetzt.
Andere Tierarten oder der Mensch sind durch die beim Hund krankheitsauslösenden Babesien nicht gefährdet. Allerdings kommen auch bei anderen Säugetieren Erkrankungen durch zumeist wirtsspezifische Babesien vor (→ Babesiose des Menschen und Systematik der Babesien).
Erreger und Verbreitung
Babesien sind Einzeller, die als Parasiten die roten Blutkörperchen befallen. Sie werden den Apicomplexa zugeordnet. Ein Abschnitt ihres Vermehrungszyklus findet im Zwischenwirt – verschiedenen Zeckenarten – statt. Die Babesiose der Hunde wird durch mehrere Babesienarten hervorgerufen, die für andere Tierarten nicht krankheitserregend sind.
Babesia canis ist eine relative große Babesienart (2–4 × 4–7 μm), die weltweit vorkommt. Man unterscheidet heute drei Unterarten, die sich hinsichtlich ihrer DNA und ihres Vektors, aber nicht morphologisch unterscheiden:
- Babesia canis canis wird durch die Auwaldzecke (Dermacentor reticularis) übertragen, die sich mittlerweile in ganz Mitteleuropa ausgebreitet hat.[2] Diese Babesien-Unterart ist im deutschsprachigen Raum am häufigsten für Erkrankungen bei Hunden verantwortlich. Ursprünglich nur in Nordafrika, Nord- und Mittelitalien, Frankreich und im südlichen Teil Ungarns und Österreichs vorkommend, gibt es mittlerweile Naturherde in Deutschland, der Schweiz, Holland und Polen. Der Erreger ist stark krankheitsauslösend.
- Babesia canis vogeli wird durch die Braune Hundezecke (Rhipicephalus sanguineus) übertragen. Infektionen mit diesem Erreger sind in Mitteleuropa selten und verlaufen mild. Verbreitet ist B. c. vogeli in Nordafrika, dem Mittelmeerraum und Frankreich.
- Babesia canis rossi wird durch Haemaphysalis leachi verbreitet und kommt nur in Afrika südlich der Sahara vor. Der Erreger ist stark krankheitsauslösend.
Das ursprüngliche Verbreitungsgebiet der Babesiose (Enzootiegebiet) innerhalb Europas beschränkte sich bis in die 1970er Jahre auf Südeuropa, so dass die Erkrankung in Deutschland nahezu ausschließlich bei Hunden nach Urlaubsreisen in diese Region auftrat.
Mit der Ausbreitung der Auwaldzecke auf ganz Mitteleuropa kommen ortsständige Krankheitsfälle auch in Deutschland vor: Etwa ein Drittel der erkrankten Hunde hatte niemals einen Auslandsaufenthalt. Die Durchseuchung der Auwaldzecken mit Babesien ist in Deutschland zwar noch relativ gering, allerdings stetig ansteigend. Etwa 0,5 % der Auwaldzecken sind Babesienträger.
Nachdem zunächst nur am Oberrhein ortsständige Infektionen beobachtet wurden, gibt es mittlerweile Enzootiegebiete im Saarland, in Rheinland-Pfalz, in den Isarauen bei München, in der Umgebung von Regensburg, in den Elbauen und in Brandenburg. Derzeit werden einige tausend Erkrankungen pro Jahr in Deutschland festgestellt. Davon sind etwa 300–400 ortsständige Infektionen, die fast alle im Saarland und am Oberrhein auftreten.
Krankheitsentstehung
Die Übertragung beim Zeckenstich dauert etwa 48 bis 72 Stunden, unter experimentellen Bedingungen konnte bereits nach 12 Stunden nach Anheften der Zecke eine Übertragung von B. c. canis nachgewiesen werden.
Durch das Anheften der Zecke an den Wirt werden durch Reizung des Nervensystems die in verschiedenen Organen ruhenden Sporozoiten aktiviert und entwickeln sich zu Kineten, die dann in die Speicheldrüsen einwandern und mit dem Zeckenspeichel in den Blutkreislauf des Hundes gelangen.
Neben der Übertragung durch Zecken ist eine Infektion von Hund zu Hund über eine Bluttransfusion oder durch Blut-Blut-Kontakte – beispielsweise bei Beißereien – möglich.
Krankheitsbild
In Deutschland tritt vor allem die akut verlaufende Form der Babesia-canis-canis-Infektion auf. Die Inkubationszeit beträgt 5 bis 7 Tage, selten kann sie bis zu drei Wochen nach dem Zeckenstich dauern.
Krankheitszeichen (Symptome) sind ein gestörtes Allgemeinbefinden und Fieber, gefolgt von Fressunlust, Gewichtsverlust und Abgeschlagenheit. Ein bis zwei Tage später kommt es aufgrund des Zerfalls der roten Blutkörperchen (Hämolyse) zu Blutarmut (Anämie), Blutharnen, Ausscheidung des Blutfarbstoffabbauprodukts Bilirubin über den Harn (Bilirubinurie) und gegebenenfalls auch Gelbsucht. Eine Leber- und Milzvergrößerung kommt häufig vor.
Bei schweren Verläufen treten eine Bauchwassersucht und Wasseransammlungen (Ödeme) sowie Haut- und Schleimhautblutungen infolge Blutplättchenmangel (Thrombozytopenie) und eine Blutgerinnung innerhalb der Blutgefäße (disseminierte intravasale Koagulopathie) auf. Entzündungen der Maul- (Stomatitis) und Magenschleimhaut (Gastritis) sowie der Muskulatur (Myositis) sind häufig. Auch eine zentralnervöse Form mit epilepsieähnlichen Anfällen, Bewegungsstörungen und Lähmungen ist möglich.
Die akute Form endet unbehandelt binnen weniger Tage mit dem Tod durch Atemnot, Anämie und Nierenversagen, welches eine gefürchtete Komplikation einer Babesiose ist. Der seltene perakute Verlauf endet ohne deutliche Symptome binnen ein bis zwei Tagen tödlich.
Diagnostik
Die Babesiose kann klinisch mit einer Vielzahl anderer fieberhafter Erkrankungen verwechselt werden. Die Diagnose ist über einen normalen Blutausstrich („Dünner Tropfen“) oder den so genannten „Dicken Tropfen“ möglich, wobei Kapillarblut sensitiver ist als venöses Blut.
Die Erreger können in der Frühphase der Infektion und in den Phasen zwischen den Vermehrungsschüben im Blut (Parasitämie) nur in geringer Zahl auftreten und damit übersehen werden. Sicher ist der Nachweis im Blutausstrich erst etwa 7 Tage nach der Infektion. Die Babesien können unter dem Mikroskop nachgewiesen werden, wobei die Giemsa-Färbung – im Gegensatz zu den üblichen Schnellfärbungen – am zuverlässigsten ist
Behandlung und Vorbeugung
Da die Krankheit ohne Behandlung schnell tödlich endet, sollte bei Verdacht unverzüglich eine Therapie eingeleitet werden. Antiprotozoika wie Imidocarb oder Diminazen sind gegen B. canis gut, gegen „kleine Babesien“ dagegen nur wenig wirksam. Imidocarb kann auch zur Prophylaxe bei Reisen in Endemiegebiete einmalig verabreicht werden – der Schutz hält etwa drei Wochen an. Eine Kombination aus Atovaquon und Azithromycin kann auch chronische Infektionen mit B. gibsoni heilen. Auch Phenamidin ist gegen „kleine Babesien“ wirksam, aber derzeit in Deutschland nicht erhältlich. In akuten Fällen ist bei einem Hämatokrit unter 20 eine Bluttransfusion oder die Gabe von Hämoglobin-Glutamer 200 angezeigt.
Die wichtigste Prophylaxe ist das Absuchen des Tieres nach Zecken nach jedem Spaziergang und deren sofortige Entfernung. Ein Schutz vor Zecken durch äußerlich anzuwendende zeckenabtötende Wirkstoffe (Akarizide wie Amitraz, Deltamethrin, Fipronil, Flumethrin oder Permethrin) ist sinnvoll, da sie auch die Gefahr des Auftretens weiterer, durch Zecken auf Hunde übertragbarer Erkrankungen wie Borreliose, Ehrlichiose, Hepatozoonose oder FSME senken.
eingestellt von: ise; Quellen- und Bildnachweis
x

Quellen- und Bildnachweis

Bildname:
Auwaldzecke – der wichtigste Überträger der Babesiose bei Hunden in Europa
Urheber:
Wikipedia/Rainer Altenkamp, Berlin
Link:
Bandwurmerkrankungen des Hundes
Bei Hunden treten eine Reihe von Bandwürmern auf, die das klinische Bild der Bandwurmerkrankungen des Hundes auslösen können. Für den Menschen ist besonders die Erkrankung durch den Dreigliedrigen Hundebandwurm von Bedeutung, der oft einfach als „Hundebandwurm“ bezeichnet wird. Bandwurmerkrankungen verlaufen bei Hunden meist ohne klinische Symptome.
Bandwurmarten
Der Gurkenkern- bzw. Kürbiskernbandwurm ist der häufigste Bandwurm beim Hund und kommt weltweit vor. Zwischenwirte sind Flöhe oder Milben.
Die Wurmeier werden von den Flohlarven aufgenommen und entwickeln sich in ihnen zu Cysticercoiden. Durch Fressen der Flöhe gelangen diese Bandwurmstadien in den Darm des Hundes und entwickeln sich dort in 20 Tagen zum adulten Bandwurm. Dieser ist 10–70 cm lang und hat eine Breite von 2–3 mm.
Durch Wechsel der Flöhe auf andere Hunde (oder Katzen) wird er in der Population weiter verbreitet. Selten werden auch Erkrankungen des Menschen, vor allem bei Kindern beobachtet. Diese nennt man Dipylidiasis. Der Dickhalsige Bandwurm ist der bei Hunden zweithäufigste Bandwurm. Der Fuchsbandwurm tritt bei Haushunden nur sehr selten auf.
Klinisches Bild
Bandwürmer lösen bei Hunden nur selten deutliche Krankheitssymptome aus. Stärkerer Befall äußert sich in Abgeschlagenheit, leichtem Durchfall und Abmagerung. Gelegentlich kann es auch zu einer Obstipation (Verstopfung) kommen.
Diagnose
Die Bandwurmglieder des Gurkenkernbandwurms können im Kot oder der Analregion auffallen. Für den Nachweis von Echinococcus ist eine mikroskopische Untersuchung des Kots zum Nachweis der Wurmeier notwendig.
Bekämpfung
Für die Behandlung infizierter Hunde ist eine regelmäßige Entwurmung, vor allem wegen der für den Menschen gefährlichen Bandwürmer anzuraten. Wirksame Mittel sind zum Beispiel Praziquantel und Epsiprantel. Für die Bekämpfung von Dipylidium caninum ist auch eine regelmäßige Prophylaxe gegen Flöhe mit Flohmitteln (z. B. Fipronil) empfehlenswert.
Die beweglichen Bandwurmglieder können am After Juckreiz hervorrufen, was zum sogenannten „Schlittenfahren“ führen kann, welches aber auch bei Erkrankung der Analbeutel auftritt.
Bandwurmarten
Der Gurkenkern- bzw. Kürbiskernbandwurm ist der häufigste Bandwurm beim Hund und kommt weltweit vor. Zwischenwirte sind Flöhe oder Milben.
Die Wurmeier werden von den Flohlarven aufgenommen und entwickeln sich in ihnen zu Cysticercoiden. Durch Fressen der Flöhe gelangen diese Bandwurmstadien in den Darm des Hundes und entwickeln sich dort in 20 Tagen zum adulten Bandwurm. Dieser ist 10–70 cm lang und hat eine Breite von 2–3 mm.
Durch Wechsel der Flöhe auf andere Hunde (oder Katzen) wird er in der Population weiter verbreitet. Selten werden auch Erkrankungen des Menschen, vor allem bei Kindern beobachtet. Diese nennt man Dipylidiasis. Der Dickhalsige Bandwurm ist der bei Hunden zweithäufigste Bandwurm. Der Fuchsbandwurm tritt bei Haushunden nur sehr selten auf.
Klinisches Bild
Bandwürmer lösen bei Hunden nur selten deutliche Krankheitssymptome aus. Stärkerer Befall äußert sich in Abgeschlagenheit, leichtem Durchfall und Abmagerung. Gelegentlich kann es auch zu einer Obstipation (Verstopfung) kommen.
Diagnose
Die Bandwurmglieder des Gurkenkernbandwurms können im Kot oder der Analregion auffallen. Für den Nachweis von Echinococcus ist eine mikroskopische Untersuchung des Kots zum Nachweis der Wurmeier notwendig.
Bekämpfung
Für die Behandlung infizierter Hunde ist eine regelmäßige Entwurmung, vor allem wegen der für den Menschen gefährlichen Bandwürmer anzuraten. Wirksame Mittel sind zum Beispiel Praziquantel und Epsiprantel. Für die Bekämpfung von Dipylidium caninum ist auch eine regelmäßige Prophylaxe gegen Flöhe mit Flohmitteln (z. B. Fipronil) empfehlenswert.
Die beweglichen Bandwurmglieder können am After Juckreiz hervorrufen, was zum sogenannten „Schlittenfahren“ führen kann, welches aber auch bei Erkrankung der Analbeutel auftritt.
eingestellt von: ise; Quellennachweis
Canine Demodikose
Die canine Demodikose ist eine häufige, durch die übermäßige Vermehrung der Haarbalgmilbe Demodex canis hervorgerufene, parasitäre Hauterkrankung der Hunde (Canidae). Sie kann örtlich begrenzt oder am ganzen Körper auftreten. Die Demodikose entsteht bei älteren Tieren nur im Zusammenhang mit Störungen des Immunsystems, bei Jungtieren ist die Entstehung der Krankheit nicht vollständig aufgeklärt.
Die Demodikose beginnt zumeist mit Haarausfall und ohne Juckreiz. Im weiteren Verlauf können sich durch eine bakterielle Sekundärinfektion stärkere Hautveränderungen bis zu einer eitrigen Hautentzündung (Pyodermie) entwickeln. Die Krankheit wird durch den mikroskopischen Nachweis der Milben festgestellt. Die Behandlung erfolgt mit milbenwirksamen Medikamenten.
Krankheitsursache
Auslöser einer Demodikose ist vor allem Demodex canis. Demodex canis ist eine schlanke, etwa 250 bis 300 µm lange und 40 µm dicke Milbe, die in den Haarbälgen (Haarfollikeln) und Talgdrüsen parasitiert. Dort ernährt sie sich von Talg, Gewebsflüssigkeit und den natürlich abgestoßenen Zellen. In geringer Zahl kommen diese Milben als Kommensale auch bei vielen klinisch gesunden Tieren vor. Die weiblichen Milben legen Eier, die sich über ein Larven- und Nymphenstadium zu den erwachsenen Milben entwickeln.
Der gesamte Entwicklungszyklus findet in den Haarbälgen statt und dauert 20 bis 35 Tage. Außerhalb des Wirtes sind Haarbalgmilben nicht überlebensfähig und sterben infolge Austrocknung schnell ab. Haarbalgmilben produzieren keinen Kot, sondern lagern Stoffwechselabbauprodukte in Zellen des Darmtrakts ein, so dass sie kaum eine Immunantwort provozieren.
Krankheitsentstehung und Verbreitung
Die Übertragung der Demodex-Milben erfolgt zumeist schon im Alter von wenigen Lebenstagen von der Hündin auf die Welpen beim Säugen. Diese Infektion bleibt aber in der Regel symptomlos.
Eine Übertragung von Hund zu Hund nach dem dritten Lebenstag gilt als unwahrscheinlich. Zum Ausbruch einer Demodikose kommt es erst viel später, wenn sich diese Milben stark vermehren. Betroffene Jungtiere scheinen keine Störungen des Immunsystems zu haben. Lediglich eine vorübergehende Verminderung der T-Zell-Immunität wird beobachtet, die unter Umständen aber nur Folge der Erkrankung ist. Bei älteren Tieren kommt es meist durch Störungen des Immunsystems (Tumore, Nebennierenüberfunktion, Schilddrüsenunterfunktion, Leishmaniose, Mangelernährung sowie Behandlung mit Glukokortikoiden, anderen Immunsuppressiva, Progesteron oder Chemotherapeutika) zu einer Demodikose.
Der Erreger verursacht bei Krankheitsausbruch eine Schädigung der beim Hund zusammengesetzten Haarfollikel (bis zu 20 Haare pro Follikel) und eine Störung der Haarbildung.
Die Demodikose tritt weltweit auf. Eine erhöhte Krankheitsneigung bestimmter Hunderassen (Rasseprädisposition) wird in Europa, im Gegensatz zu den Vereinigten Staaten, nicht beobachtet. In Amerika sind vor allem Englische Bulldogge, Französische Bulldogge, Mops, Dobermann, Deutscher Schäferhund und einige Terrier betroffen. Dies wird dadurch erklärt, dass in Europa immungeschwächte Tiere („Kümmerer“) nicht zur Zucht verwendet werden. Darüber hinaus scheint es eine individuelle genetische Prädisposition zu geben.
Eine Übertragung auf andere Spezies findet nicht statt, da Haarbalgmilben streng wirtsspezifisch sind.
Klinisches Bild
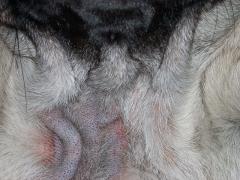
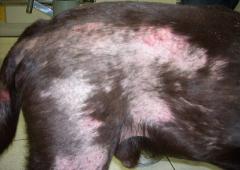
Das erste Zeichen einer Demodikose durch Demodex canis ist zumeist Haarausfall (Alopezie), der nur an umschriebenen Stellen oder auch am ganzen Körper (generalisiert) auftreten kann. Häufig tritt an den haarlosen Stellen eine vermehrte Talg- (Seborrhö) oder Schuppenbildung auf. In einigen Fällen können letztere Symptome auch ohne Haarverlust auftreten. Später kann es zu einer grauen Verfärbung der geschädigten Areale kommen. Bis zu diesem Stadium ist zumeist kein Juckreiz vorhanden.
Bei Jungtieren (jünger als 18 Monate) beginnen die Veränderungen zumeist im Gesichtsbereich („Brillenbildung“, Lefzen, Kinn) und/oder an den Gliedmaßen. Zumeist heilt diese Erkrankung auch ohne Behandlung nach wenigen Wochen ab, sie kann sich aber auch weiter ausdehnen und in eine generalisierte Demodikose übergehen.
Im weiteren Verlauf ist das klinische Bild durch eine bakterielle Sekundärinfektion, vor allem mit Staphylokokken, seltener auch mit Proteus, Klebsiellen oder Escherichia coli gekennzeichnet. Es kommt zu einer Follikulitis, Furunkulose und übermäßigen Verhornung (Hyperkeratose). Gelegentlich kann sich dieses Stadium der Erkrankung auch durch Pusteln manifestieren. Bei tiefem Eindringen der Bakterien in die Haut entwickelt sich eine eitrige Hautentzündung (Pyodermie) mit Bildung von Krusten und Schwellungen der Lymphknoten.
Sonderformen sind der Befall der Haut der Füße und des Ohrs. Der Befall der Füße (Pododemodikose) äußert sich in Rötung und Schwellung (Ödem) im Zwischenzehenbereich; in ausgeprägten Fällen entwickeln sich Granulome und Fisteln, so dass das Bild einer chronischen Pododermatitis entsteht. Der Befall des äußeren Gehörgangs (Otodemodikose) wird vor allem bei generalisierter Demodikose beobachtet und ist durch ein bräunliches Sekret gekennzeichnet.
Infektionen mit anderen Demodex-Milben
Demodex-injai-Infektionen äußern sich zumeist mit erhöhter Talgproduktion („fettige Haut“), schlechter Haarqualität mit schütterem Haar und vor allem am Rücken auftretendem Juckreiz. Auch Papeln, Pusteln oder „Mitesser“ können auftreten. Diese Form der Demodikose wird vor allem bei Terriern beobachtet. Demodex-cornei-Infektionen zeigen sich in Rötungen der Haut, Schuppenbildung und ausgeprägtem Juckreiz.
Behandlung
Eine lokale Demodikose bei Jungtieren bildet sich in 90 % der Fälle wieder spontan zurück. Ob eine Behandlung sinnvoll ist oder nicht, ist in der Literatur umstritten. Zum einen wird sie empfohlen, um eine Generalisierung zu vermeiden, zum anderen wird empfohlen, gerade die mögliche Generalisierung abzuwarten, um sie als Zuchtausschlusskriterium (siehe unten) nutzen zu können. Eine lokale äußerliche (topische) Behandlung zum Beispiel durch Auftragen eines Gels mit Benzoylperoxid, Chlorhexidin oder Rotenon ist dabei zumeist ausreichend. Benzoylperoxid dringt zwar gut in die Haarfollikel ein, wirkt allerdings stark austrocknend und zum Teil hautreizend.
Eine ausgeprägte Demodikose ist generell mit einer Ganzkörperbehandlung zu therapieren.
Sowohl bei lokaler als auch systemischer Demodikose hat sich die regelmäßige Waschbehandlung mit Amitraz bewährt.
Einige Zwerghunderassen (Chihuahua, Malteser) reagieren allerdings sehr empfindlich auf diesen Wirkstoff, so dass der Einsatz bei diesen nicht empfohlen wird. Bei starkem Befall wird bei langhaarigen Hunden eine vollständige Schur empfohlen, da der Wirkstoff die Haut gut benetzen muss, um tief genug in die Haarbälge eindringen zu können. Bei starker bakterieller Sekundärinfektion ist zunächst diese zu behandeln, z. B. durch Scheren der betroffenen Partien, Reinigen mit desinfizierend wirkenden Waschlösungen und systemischer Verabreichung von Antibiotika, da Amitraz nicht auf größere Wunden aufgebracht werden sollte.
Seit Juni 2009 ist auch ein Spot-On-Präparat mit Amitraz zur Behandlung der Demodikose zugelassen, das nur 14-täglich aufgetragen werden muss. Insbesondere bei lokaler Demodikose ist eine 14-tägliche Therapiekontrolle sinnvoll, um einem zu frühen Abbruch der Behandlung und damit der Gefahr der Entstehung einer generalisierten Demodikose vorzubeugen. Ein sich abzeichnender Behandlungserfolg ist anhand der Abnahme der Zahl lebender Milben, der Zunahme verkrüppelter Milben und der Abnahme der Larven sichtbar.
Eine vollständige Ausheilung wird durch nachgewachsene Haare und fehlenden Nachweis lebender Milben angezeigt und gelingt mit Amitraz etwa in 80 % der Fälle. In etwa 40 % der Fälle treten Nebenwirkungen wie Abgeschlagenheit und Juckreiz auf, die durch stärkere Verdünnung oder Verminderung der Behandlungsfrequenz reduziert werden können. Gelegentlich können auch schwerere Nebenwirkungen wie Fressunlust, Ataxie sowie vermehrter Durst und Harnabsatz auftreten. Da Amitraz auch zu einem Anstieg des Blutzuckerspiegels führt, ist der Einsatz bei zuckerkranken Hunden kontraindiziert.
Behandlungsaussicht
Die Behandlung ist bei lokalisierter Demodikose zumeist erfolgreich. Von einer erfolgreichen Therapie wird ausgegangen, wenn sich in zwei, im Abstand von zwei Wochen aufeinanderfolgenden Hautuntersuchungen von vier bis fünf verschiedenen Stellen keine lebenden Milben mehr nachweisen lassen.
Schwere, generalisierte Formen und die Pododemodikose können sich als therapieresistent erweisen, insbesondere wenn nicht behebbare Störungen des Immunsystems oder fördernde Primärleiden vorliegen. Die Gefahr von Rezidiven sinkt deutlich, wenn das betroffene Tier ein Jahr symptomfrei bleibt. Bei einigen Tieren kann eine Symptomfreiheit nur durch lebenslange Gabe von Amitraz oder Ivermectin erreicht werden.
Die Demodikose beginnt zumeist mit Haarausfall und ohne Juckreiz. Im weiteren Verlauf können sich durch eine bakterielle Sekundärinfektion stärkere Hautveränderungen bis zu einer eitrigen Hautentzündung (Pyodermie) entwickeln. Die Krankheit wird durch den mikroskopischen Nachweis der Milben festgestellt. Die Behandlung erfolgt mit milbenwirksamen Medikamenten.
Krankheitsursache
Auslöser einer Demodikose ist vor allem Demodex canis. Demodex canis ist eine schlanke, etwa 250 bis 300 µm lange und 40 µm dicke Milbe, die in den Haarbälgen (Haarfollikeln) und Talgdrüsen parasitiert. Dort ernährt sie sich von Talg, Gewebsflüssigkeit und den natürlich abgestoßenen Zellen. In geringer Zahl kommen diese Milben als Kommensale auch bei vielen klinisch gesunden Tieren vor. Die weiblichen Milben legen Eier, die sich über ein Larven- und Nymphenstadium zu den erwachsenen Milben entwickeln.
Der gesamte Entwicklungszyklus findet in den Haarbälgen statt und dauert 20 bis 35 Tage. Außerhalb des Wirtes sind Haarbalgmilben nicht überlebensfähig und sterben infolge Austrocknung schnell ab. Haarbalgmilben produzieren keinen Kot, sondern lagern Stoffwechselabbauprodukte in Zellen des Darmtrakts ein, so dass sie kaum eine Immunantwort provozieren.
Krankheitsentstehung und Verbreitung
Die Übertragung der Demodex-Milben erfolgt zumeist schon im Alter von wenigen Lebenstagen von der Hündin auf die Welpen beim Säugen. Diese Infektion bleibt aber in der Regel symptomlos.
Eine Übertragung von Hund zu Hund nach dem dritten Lebenstag gilt als unwahrscheinlich. Zum Ausbruch einer Demodikose kommt es erst viel später, wenn sich diese Milben stark vermehren. Betroffene Jungtiere scheinen keine Störungen des Immunsystems zu haben. Lediglich eine vorübergehende Verminderung der T-Zell-Immunität wird beobachtet, die unter Umständen aber nur Folge der Erkrankung ist. Bei älteren Tieren kommt es meist durch Störungen des Immunsystems (Tumore, Nebennierenüberfunktion, Schilddrüsenunterfunktion, Leishmaniose, Mangelernährung sowie Behandlung mit Glukokortikoiden, anderen Immunsuppressiva, Progesteron oder Chemotherapeutika) zu einer Demodikose.
Der Erreger verursacht bei Krankheitsausbruch eine Schädigung der beim Hund zusammengesetzten Haarfollikel (bis zu 20 Haare pro Follikel) und eine Störung der Haarbildung.
Die Demodikose tritt weltweit auf. Eine erhöhte Krankheitsneigung bestimmter Hunderassen (Rasseprädisposition) wird in Europa, im Gegensatz zu den Vereinigten Staaten, nicht beobachtet. In Amerika sind vor allem Englische Bulldogge, Französische Bulldogge, Mops, Dobermann, Deutscher Schäferhund und einige Terrier betroffen. Dies wird dadurch erklärt, dass in Europa immungeschwächte Tiere („Kümmerer“) nicht zur Zucht verwendet werden. Darüber hinaus scheint es eine individuelle genetische Prädisposition zu geben.
Eine Übertragung auf andere Spezies findet nicht statt, da Haarbalgmilben streng wirtsspezifisch sind.
Klinisches Bild
Das erste Zeichen einer Demodikose durch Demodex canis ist zumeist Haarausfall (Alopezie), der nur an umschriebenen Stellen oder auch am ganzen Körper (generalisiert) auftreten kann. Häufig tritt an den haarlosen Stellen eine vermehrte Talg- (Seborrhö) oder Schuppenbildung auf. In einigen Fällen können letztere Symptome auch ohne Haarverlust auftreten. Später kann es zu einer grauen Verfärbung der geschädigten Areale kommen. Bis zu diesem Stadium ist zumeist kein Juckreiz vorhanden.
Bei Jungtieren (jünger als 18 Monate) beginnen die Veränderungen zumeist im Gesichtsbereich („Brillenbildung“, Lefzen, Kinn) und/oder an den Gliedmaßen. Zumeist heilt diese Erkrankung auch ohne Behandlung nach wenigen Wochen ab, sie kann sich aber auch weiter ausdehnen und in eine generalisierte Demodikose übergehen.
Im weiteren Verlauf ist das klinische Bild durch eine bakterielle Sekundärinfektion, vor allem mit Staphylokokken, seltener auch mit Proteus, Klebsiellen oder Escherichia coli gekennzeichnet. Es kommt zu einer Follikulitis, Furunkulose und übermäßigen Verhornung (Hyperkeratose). Gelegentlich kann sich dieses Stadium der Erkrankung auch durch Pusteln manifestieren. Bei tiefem Eindringen der Bakterien in die Haut entwickelt sich eine eitrige Hautentzündung (Pyodermie) mit Bildung von Krusten und Schwellungen der Lymphknoten.
Sonderformen sind der Befall der Haut der Füße und des Ohrs. Der Befall der Füße (Pododemodikose) äußert sich in Rötung und Schwellung (Ödem) im Zwischenzehenbereich; in ausgeprägten Fällen entwickeln sich Granulome und Fisteln, so dass das Bild einer chronischen Pododermatitis entsteht. Der Befall des äußeren Gehörgangs (Otodemodikose) wird vor allem bei generalisierter Demodikose beobachtet und ist durch ein bräunliches Sekret gekennzeichnet.
Infektionen mit anderen Demodex-Milben
Demodex-injai-Infektionen äußern sich zumeist mit erhöhter Talgproduktion („fettige Haut“), schlechter Haarqualität mit schütterem Haar und vor allem am Rücken auftretendem Juckreiz. Auch Papeln, Pusteln oder „Mitesser“ können auftreten. Diese Form der Demodikose wird vor allem bei Terriern beobachtet. Demodex-cornei-Infektionen zeigen sich in Rötungen der Haut, Schuppenbildung und ausgeprägtem Juckreiz.
Behandlung
Eine lokale Demodikose bei Jungtieren bildet sich in 90 % der Fälle wieder spontan zurück. Ob eine Behandlung sinnvoll ist oder nicht, ist in der Literatur umstritten. Zum einen wird sie empfohlen, um eine Generalisierung zu vermeiden, zum anderen wird empfohlen, gerade die mögliche Generalisierung abzuwarten, um sie als Zuchtausschlusskriterium (siehe unten) nutzen zu können. Eine lokale äußerliche (topische) Behandlung zum Beispiel durch Auftragen eines Gels mit Benzoylperoxid, Chlorhexidin oder Rotenon ist dabei zumeist ausreichend. Benzoylperoxid dringt zwar gut in die Haarfollikel ein, wirkt allerdings stark austrocknend und zum Teil hautreizend.
Eine ausgeprägte Demodikose ist generell mit einer Ganzkörperbehandlung zu therapieren.
Sowohl bei lokaler als auch systemischer Demodikose hat sich die regelmäßige Waschbehandlung mit Amitraz bewährt.
Einige Zwerghunderassen (Chihuahua, Malteser) reagieren allerdings sehr empfindlich auf diesen Wirkstoff, so dass der Einsatz bei diesen nicht empfohlen wird. Bei starkem Befall wird bei langhaarigen Hunden eine vollständige Schur empfohlen, da der Wirkstoff die Haut gut benetzen muss, um tief genug in die Haarbälge eindringen zu können. Bei starker bakterieller Sekundärinfektion ist zunächst diese zu behandeln, z. B. durch Scheren der betroffenen Partien, Reinigen mit desinfizierend wirkenden Waschlösungen und systemischer Verabreichung von Antibiotika, da Amitraz nicht auf größere Wunden aufgebracht werden sollte.
Seit Juni 2009 ist auch ein Spot-On-Präparat mit Amitraz zur Behandlung der Demodikose zugelassen, das nur 14-täglich aufgetragen werden muss. Insbesondere bei lokaler Demodikose ist eine 14-tägliche Therapiekontrolle sinnvoll, um einem zu frühen Abbruch der Behandlung und damit der Gefahr der Entstehung einer generalisierten Demodikose vorzubeugen. Ein sich abzeichnender Behandlungserfolg ist anhand der Abnahme der Zahl lebender Milben, der Zunahme verkrüppelter Milben und der Abnahme der Larven sichtbar.
Eine vollständige Ausheilung wird durch nachgewachsene Haare und fehlenden Nachweis lebender Milben angezeigt und gelingt mit Amitraz etwa in 80 % der Fälle. In etwa 40 % der Fälle treten Nebenwirkungen wie Abgeschlagenheit und Juckreiz auf, die durch stärkere Verdünnung oder Verminderung der Behandlungsfrequenz reduziert werden können. Gelegentlich können auch schwerere Nebenwirkungen wie Fressunlust, Ataxie sowie vermehrter Durst und Harnabsatz auftreten. Da Amitraz auch zu einem Anstieg des Blutzuckerspiegels führt, ist der Einsatz bei zuckerkranken Hunden kontraindiziert.
Behandlungsaussicht
Die Behandlung ist bei lokalisierter Demodikose zumeist erfolgreich. Von einer erfolgreichen Therapie wird ausgegangen, wenn sich in zwei, im Abstand von zwei Wochen aufeinanderfolgenden Hautuntersuchungen von vier bis fünf verschiedenen Stellen keine lebenden Milben mehr nachweisen lassen.
Schwere, generalisierte Formen und die Pododemodikose können sich als therapieresistent erweisen, insbesondere wenn nicht behebbare Störungen des Immunsystems oder fördernde Primärleiden vorliegen. Die Gefahr von Rezidiven sinkt deutlich, wenn das betroffene Tier ein Jahr symptomfrei bleibt. Bei einigen Tieren kann eine Symptomfreiheit nur durch lebenslange Gabe von Amitraz oder Ivermectin erreicht werden.
eingestellt von: ise; Quellen- und Bildnachweis
Cheyletiellose
Cheyletiellose ist eine parasitäre Erkrankung der Haut, die auch bei Hunden vorkommt, aber auch den Menschen befallen kann. Sie wird durch Milben der Gattung Cheyletiella hervorgerufen.
Erreger
Die Milben sind bis zu 0,4 mm groß, haben 4 Beinpaare und leben auf dem Wirt, ohne ihn durch Zwischenstadien zu verlassen, so dass der gesamte Zyklus auf dem betroffenen Tier abläuft. Die Ansteckung erfolgt durch direkten oder indirekten Kontakt.
Klinik
Eine Cheyletiellose ist hochansteckend und spielt vor allem in größeren Haltungen eine Rolle.
Da sich Cheleytiellen vorwiegend von Hautsekreten und anderen harmlosen Hautbewohnern ernähren, kann der Befall auch symptomlos bleiben. Vor allem bei Jungtieren können typische kleine trockene Schuppen mit oder ohne Juckreiz auftreten. Bei Juckreiz können durch Selbstverletzung auch schwerere Hautveränderungen entstehen. Menschen kann die Krankheit auch befallen und dabei heftige Veränderungen in Form juckender Papeln am Bauch oder den Armen auslösen, die aber ohne weiteren Kontakt mit infizierten Tieren nach etwa drei Wochen abheilen.
Schon bei geringer Vergrößerung sind die weißen Milben und die an den Haaren haftenden Nissen gut sichtbar. Da die Milben sehr beweglich sind und auf der Hautoberfläche leben, eignet sich zum Nachweis vor allem ein Abklatschpräparat mit einem durchsichtigen Klebestreifen, das anschließend mikroskopisch untersucht wird.
Zur Bekämpfung können akarizid wirkende Wirkstoffe, wie Pyrethroide, Amitraz, Ivermectin, Selamectin oder Doramectin eingesetzt werden.
Erreger
Die Milben sind bis zu 0,4 mm groß, haben 4 Beinpaare und leben auf dem Wirt, ohne ihn durch Zwischenstadien zu verlassen, so dass der gesamte Zyklus auf dem betroffenen Tier abläuft. Die Ansteckung erfolgt durch direkten oder indirekten Kontakt.
Klinik
Eine Cheyletiellose ist hochansteckend und spielt vor allem in größeren Haltungen eine Rolle.
Da sich Cheleytiellen vorwiegend von Hautsekreten und anderen harmlosen Hautbewohnern ernähren, kann der Befall auch symptomlos bleiben. Vor allem bei Jungtieren können typische kleine trockene Schuppen mit oder ohne Juckreiz auftreten. Bei Juckreiz können durch Selbstverletzung auch schwerere Hautveränderungen entstehen. Menschen kann die Krankheit auch befallen und dabei heftige Veränderungen in Form juckender Papeln am Bauch oder den Armen auslösen, die aber ohne weiteren Kontakt mit infizierten Tieren nach etwa drei Wochen abheilen.
Schon bei geringer Vergrößerung sind die weißen Milben und die an den Haaren haftenden Nissen gut sichtbar. Da die Milben sehr beweglich sind und auf der Hautoberfläche leben, eignet sich zum Nachweis vor allem ein Abklatschpräparat mit einem durchsichtigen Klebestreifen, das anschließend mikroskopisch untersucht wird.
Zur Bekämpfung können akarizid wirkende Wirkstoffe, wie Pyrethroide, Amitraz, Ivermectin, Selamectin oder Doramectin eingesetzt werden.
eingestellt von: ise; Quellen- und Bildnachweis
Dipylidiasis
Dipylidiasis oder auch Dipylidiose ist eine Erkrankung, die durch den Gurkenkernbandwurm des Hundes verursacht wird. Sie kann auf den Menschen übertragen werden und ist daher eine Zoonose.
Entwicklungszyklus
Der normale Endwirt dieses Bandwurms ist der Hund, bei dem er der häufigste Bandwurm ist und weltweit vorkommt.
Zwischenwirte sind Flöhe oder Milben (Trichodectes). Die Wurmeier werden von den Flohlarven aufgenommen und entwickeln sich in ihnen zu Cysticercoiden. Durch Fressen der Flöhe gelangen diese Bandwurmstadien in den Darm des Hundes und entwickeln sich dort in 20 Tagen zum adulten Bandwurm. Dieser ist 10–70 cm lang und hat Breite von 2–3 mm. Durch Wechsel der Flöhe auf andere Hunde (oder Katzen) wird er in der Population weiter verbreitet.
Erkrankung beim Menschen
Gelegentlich wurden Erkrankungen beim Menschen beschrieben, wobei eine, meist versehentliche Aufnahme von Flöhen über den Mund die Ursache ist. Die Erkrankung tritt vor allem bei Kindern unter 8 Jahren auf.
Die Erkrankung bleibt meist symptomlos, gelegentlich zeigen sich Störungen des Verdauungstrakts (Bauchschmerz mit oder ohne Durchfall, Appetitlosigkeit). Auch allergische Reaktionen mit Juckreiz wurden beobachtet. Sehr selten, nur bei massivem Befall, tritt eine Verstopfung durch die Bandwürmer auf.
Die Diagnose erfolgt durch den Nachweis der Bandwurmeier im Stuhl. Auch reiskornähnliche Bandwurmglieder können im Stuhl auftreten. Die Behandlung kann mit Antihelminthika (z. B. Praziquantel) erfolgen.
Die Vorbeugung gegen die Erkrankung ist durch Hygiene beim Umgang mit dem Hund und in der konsequenten Flohbekämpfung und Entwurmung des Hundes (auch prophylaktisch) möglich.
Entwicklungszyklus
Der normale Endwirt dieses Bandwurms ist der Hund, bei dem er der häufigste Bandwurm ist und weltweit vorkommt.
Zwischenwirte sind Flöhe oder Milben (Trichodectes). Die Wurmeier werden von den Flohlarven aufgenommen und entwickeln sich in ihnen zu Cysticercoiden. Durch Fressen der Flöhe gelangen diese Bandwurmstadien in den Darm des Hundes und entwickeln sich dort in 20 Tagen zum adulten Bandwurm. Dieser ist 10–70 cm lang und hat Breite von 2–3 mm. Durch Wechsel der Flöhe auf andere Hunde (oder Katzen) wird er in der Population weiter verbreitet.
Erkrankung beim Menschen
Gelegentlich wurden Erkrankungen beim Menschen beschrieben, wobei eine, meist versehentliche Aufnahme von Flöhen über den Mund die Ursache ist. Die Erkrankung tritt vor allem bei Kindern unter 8 Jahren auf.
Die Erkrankung bleibt meist symptomlos, gelegentlich zeigen sich Störungen des Verdauungstrakts (Bauchschmerz mit oder ohne Durchfall, Appetitlosigkeit). Auch allergische Reaktionen mit Juckreiz wurden beobachtet. Sehr selten, nur bei massivem Befall, tritt eine Verstopfung durch die Bandwürmer auf.
Die Diagnose erfolgt durch den Nachweis der Bandwurmeier im Stuhl. Auch reiskornähnliche Bandwurmglieder können im Stuhl auftreten. Die Behandlung kann mit Antihelminthika (z. B. Praziquantel) erfolgen.
Die Vorbeugung gegen die Erkrankung ist durch Hygiene beim Umgang mit dem Hund und in der konsequenten Flohbekämpfung und Entwurmung des Hundes (auch prophylaktisch) möglich.
eingestellt von: ise; Quellennachweis
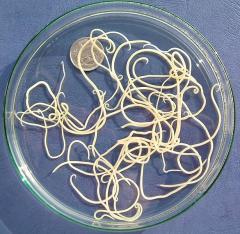
Fadenwurminfektionen des Hundes
Fadenwurminfektionen des Hundes – die Ansteckung (Infektion, auch Infestation) von Hunden mit parasitisch lebenden Fadenwürmern sind neben dem Bandwurmbefall und den Infektionen mit Einzellern häufige Parasitosen in der tierärztlichen Praxis.
Fadenwürmer besiedeln als sogenannte „Innenschmarotzer“ verschiedene innere Organe – die meisten von ihnen den Verdauungstrakt – und die Haut. Bislang sind bei Hunden etwa 30 verschiedene Fadenwurmarten nachgewiesen worden; sie sind im Wesentlichen auch bei wildlebenden Hundearten zu finden. Die Mehrzahl davon ruft aber bei erwachsenen Tieren häufig keine oder nur geringe Krankheitserscheinungen hervor.
Die Infektion muss sich also nicht zwangsläufig auch in einer Wurmerkrankung äußern. Für die meisten Fadenwürmer lässt sich eine Infektion durch eine Untersuchung des Kots auf Eier oder Larven nachweisen. Von gesundheitspolitischer Bedeutung ist in Mitteleuropa vor allem der Befall mit dem Hundespulwurm und dem Hundehakenwurm, da sie auch auf den Menschen übergehen können (Zoonose).
Eine regelmäßige Entwurmung kann die Befallshäufigkeit und damit die Infektionsgefahr für Menschen und Hunde deutlich reduzieren.
Parasitosen des Verdauungstrakts
Spulwurmbefall
Bei Hunden treten zwei Spulwurmarten auf: Toxocara canis und Toxascaris leonina.
Während die Infektion mit T. leonina nur sehr selten klinische Erscheinungen wie Durchfall hervorruft, ist die krankheitsauslösende Wirkung von T. canis deutlich stärker.
Bei Welpen treten ein herabgesetztes Allgemeinbefinden, struppiges Fell, Zurückbleiben im Wachstum, abwechselnd Durchfall und Verstopfung, ein aufgetriebener Bauch („Wurmbauch“) und Blutarmut auf. Komplikationen des T.-canis-Befalls mit teilweise tödlichem Ausgang sind Darmverschluss durch Wurmknäuel, Dünndarmdurchbruch, Lungenentzündung, Leberentzündung oder neurologische Erscheinungen durch verirrte Wanderlarven im Zentralnervensystem.
Die Diagnose kann bei Würmern in Erbrochenem bereits ohne Spezialuntersuchungen gestellt werden. Relativ sicher kann ein Spulwurmbefall durch den mikroskopischen Nachweis der über das Flotationsverfahren aus dem Kot herausgelösten Eier nachgewiesen werden, allerdings erst nach Ablauf der Präpatenz.
Hakenwurmbefall (Ankylostomyasis)
Bei Hunden kommen vor allem zwei Hakenwurmarten vor: Ancylostoma caninum und Uncinaria stenocephala. Sie parasitieren im Dünndarm und verursachen durch das Saugen von Blut eine Blutarmut sowie Schädigungen der Darmschleimhaut.
Die Würmer haben mit etwa 5–15 mm nur etwa ein Zehntel der Länge von Spulwürmern, ein hakenförmig abgewinkeltes Vorderende (daher der Name „Hakenwurm“) und eine große Mundkapsel mit Schneidplatten.
Während der Befall mit U. stenocephala häufig nur geringe Krankheitserscheinungen wie Durchfall verursacht, kann der Befall mit A. caninum vor allem bei Welpen schwere Krankheitsbilder verursachen. Dabei können blutiger Durchfall, starke Abgeschlagenheit und Blutarmut auftreten, teilweise mit akutem oder perakuten Verlauf und plötzlichen Todesfällen.
Bei chronischem Verlauf bleiben die Jungtiere im Wachstum zurück, sind teilnahmslos, zeigen mangelnden Appetit, Durchfall und Abmagerung. Eher selten tritt eine Lungenentzündung durch wandernde Larven auf. Ein Hakenwurmbefall kann durch den Nachweis der Eier im Kot mittels Flotationsverfahren diagnostiziert werden.
Peitschenwurmbefall (Trichuriasis)
Die krankheitsauslösende Wirkung von T. vulpis ist mittelgradig. Befallene Hunde zeigen Durchfall, der blutig, bei weniger schwerem Verlauf mit Schleim durchsetzt ist. Die Tiere magern ab, Jungtiere bleiben im Wachstum zurück, bei starkem Befall kann sich eine Blutarmut entwickeln. Eine sichere Diagnose kann nur über den Einachweis im Kot mittels Flotationsverfahren gestellt werden.
Zwergfadenwurmbefall (Strongyloidiasis)
Die Infektion mit dem Zwergfadenwurm Strongyloides canis kann durch Aufnahme infektiöser Larven über die Muttermilch, perorale Aufnahme oder durch aktives Eindringen der Larven durch die Haut erfolgen. Eine Autoinfektion, also die Infektion des gleichen Tieres durch von ihm ausgeschiedene Larven, ist möglich. S. canis parasitiert im Dünndarm. Die Eier sind etwa 50 µm lang und enthalten bei Ausscheidung mit dem Kot bereits die infektiöse Larve.
Die Strongyloidiasis verursacht bei Welpen akuten bis chronischen Durchfall, gelegentlich auch eine Verstopfung. Die Diagnose kann durch den Nachweis der Eier im Kot mittels Flotationsverfahren gestellt werden.
Magenwurmbefall
Magenwürmer gehören zu einer weltweit verbreiteten Gattung von Fadenwürmern, welche die Schleimhaut von Magen und Zwölffingerdarm befallen können.
Die Magenwürmer verursachen Schäden an der Magenschleimhaut, was zu Gastritis, Blutungen und chronischem Erbrechen führt.
Bei starkem Befall kommt es zu Gewichtsverlust und Blutarmut. Der Nachweis der Eier im Kot mit dem Flotationsverfahren ist unsicher, da sie kaum aufschwemmen. Daher gibt es keine systematischen Untersuchungen zur Vorkommenshäufigkeit. Eine sichere Diagnose kann mittels Magenspülproben oder einer Magenspiegelung gestellt werden.
Speiseröhrenwurmbefall
Die Würmer können während ihrer Wanderung gelegentlich ein Aortenaneurysma verursachen, oft sind befallene Hunde jedoch symptomlos. In der Speiseröhre selbst verursacht S. lupi eine granulomatöse Gewebsreaktion, welche ohne Behandlung sehr oft entartet und dann verschiedene bösartige Tumoren bildet.
Durch die tumorbedingte Raumforderung im Brustkorb kann es zusätzlich auch zu einer hypertrophischen Osteopathie kommen.
Parasitosen der Atemwege
Lungenhaarwurmbefall (Capillariasis)
Der Lungenwurm Crenosoma vulpis ist bis zu 1,6 cm lang und wird indirekt über das Fressen von Zwischenwirten wie Schnecken übertragen. Klinisch ist eine Infektion durch chronischen Husten gekennzeichnet und ähnelt einer allergischen Bronchitis. Der Nachweis von C. vulpis in Kotproben mit Standardflotationsverfahren ist relativ unsicher.
Filaroididae
Kommt beim Hund relativ selten vor. Das gleichzeitige Auftreten ähnlicher Symptome bei der Mutter und ihrer Welpen ist ein Hinweis auf eine solche Infektion. Gelegentlich kann bei Belastung eine anfallsartige Atemnot auftreten. Fieber tritt zumeist nicht auf.
Zur Diagnose kann der Nachweis von Knötchen mittels Lungenspiegelung, eventuell auch auf Röntgenbildern des Brustkorbs, sowie der Larven in Lungenspülflüssigkeit oder Luftröhrenabstrichen genutzt werden. Der Nachweis von Larven im Kot mittels Flotationsverfahren ist unsicher, zumal die Larven nur unregelmäßig über den Kot ausgeschieden werden, während der relativ langen Präpatenz überhaupt nicht.
Parasitosen des Blutkreislaufs
Herzwurmbefall (Dirofilariose)
Befallene Tiere zeigen mit der Entwicklung der reifen Würmer, also erst etwa sechs Monate nach der Infektion, eine reduzierte Leistungsfähigkeit und ermüden schnell. Es entwickelt sich eine Rechtsherzinsuffizienz mit Überlastung und Erweiterung der rechten Herzseite, die sich in Atemnot, Husten und der Bildung von Ödemen äußert. Infolge der Herzinsuffizienz kann auch ein Leber- und Nierenversagen entstehen.
Angiostrongylose
Der französische Herzwurm (Angiostrongylus vasorum) ist ein Parasit des Lungengefäßstamms, der Lungenarterien und der rechten Herzkammer. Klinisch zeigen befallene Hunde eine langsam fortschreitende Einschränkung der Herz- und/oder Lungenfunktion. Chronischer Husten, Atemnot, Nahrungsverweigerung und Gewichtsabnahme sind ebenfalls häufige Symptome.
Riesennierenwurmbefall
Der Riesennierenwurm ist der größte bekannte parasitische Fadenwurm und kann beim Hund die Niere, gelegentlich auch die Bauchhöhle befallen. Weibliche Würmer erreichen Längen von über einem Meter bei einem Durchmesser von bis zu 12 mm; männliche Würmer messen 20 cm auf 6–8 mm. Beide Geschlechter haben eine blutrote Farbe.
Bei Hunden verbleibt der Parasit allerdings recht häufig in der Bauchhöhle, was für den Hund weniger gravierende Folgen hat als ein Befall der Niere. Die befallene Niere wird durch den Parasiten langsam zerstört, der dabei üblicherweise auch das Nierenbecken perforiert. Da Eier im Urin sehr selten auftreten, ist deren Nachweis zur Diagnostik ungeeignet. Ein Nierenwurmbefall kann mittels Sonografie nachgewiesen werden.
Harnblasenhaarwurmbefall
Der Harnblasenhaarwurm ist 13 bis 60 mm lang und besiedelt die Harnblase, gelegentlich auch den Harnleiter und das Nierenbecken.
Bei Hunden in größeren Zwingern können bis zu drei Viertel der Tiere befallen sein. C. plica ruft selten Krankheitserscheinungen hervor. Bei stärkerem Befall kann es zu einer Harnblasenentzündung mit Harndrang und Harninkontinenz kommen. Die Diagnose kann durch den Einachweis im Urin gestellt werden, allerdings aufgrund der langen Präpatenz nicht bei Tieren, die jünger als acht Monate sind.
Parasitosen der Haut
Peloderose
Die Läsionen sind normalerweise auf diejenigen Hautteile beschränkt, die in direktem Kontakt mit dem infektiösen Material waren, meistens also Bauch, Unterbrust und Extremitäten. Die betroffene Haut ist gerötet, mäßig bis stark entzündet und teilweise bis völlig haarlos. Es besteht ein ausgeprägter Juckreiz, der zu weiteren Hautläsionen (Krustenbildung) und bakteriellen Sekundärinfektionen führen kann. Normalerweise ist die Krankheit selbstlimitierend, auch weil der Hund für die Würmer einen Fehlwirt darstellt.
Kutane Dirofilariose
Dirofilaria repens ist ein Parasit des Unterhautgewebes bei Hunden. Als Zwischenwirt und Überträger fungieren Stechmücken. Er kommt vor allem in Süd-, südlichem Ost- und Westeuropa sowie weiten Teilen Asiens vor, breitet sich aber immer weiter nach Nordeuropa aus und wird auch in Deutschland zunehmend nachgewiesen.
Der Befall mit D. repens verursacht gelegentlich Hautknoten, Schwellungen, Juckreiz, Abszesse und Haarausfall, verläuft aber oft auch völlig ohne klinische Symptome.
Thelaziose
Die Thelaziose wird durch Vertreter der Gattung Thelazia hervorgerufen. Es handelt sich um weißliche Fadenwürmer von etwa 1,5 cm Länge, in Deutschland eher selten. Thelazien parasitieren am Augapfel unter der Nickhaut sowie in den Tränenwegen und verursachen eine Bindehautentzündung und vermehrten Tränenfluss.
Auch eine Verlegung der Tränenwege oder eine Hornhautentzündung kann auftreten. Bei starkem Befall sind die Würmer bereits mit bloßem Auge sichtbar. Eine sichere Diagnose kann durch den Nachweis der Würmer oder ihrer Larven in Augenspülproben oder einem Bioptat der Tränendrüse erfolgen.
Onchozerkose
Erreger der Onchozerkose der Hunde ist Onchocerca lupi. Die Erkrankung kommt in Nordamerika und einigen Ländern Europas (Griechenland, Ungarn) vor, ist aber selten.
Die Würmer rufen erbsen- bis bohnengroße granulomatöse Knötchen in der Sclera, der Augenumgebung und Bindehaut hervor. Unter Umständen kann sich eine lymphoplasmazytäre Entzündung der mittleren Augenhaut entwickeln. Die Diagnose kann durch den Nachweis der Würmer in den Knötchen gestellt werden.
Bekämpfung
Die meisten Infektionen sind für erwachsene Hunde eher harmlos, da sich bei intaktem Immunsystem ein Erreger-Wirt-Gleichgewicht einstellt. Da aber einige von ihnen gesundheitliche Störungen auslösen können und einige auch eine potentielle Gefahr für den Menschen darstellen, sind regelmäßige Wurmkuren bei Hunden durchaus sinnvoll. Vor allem für Hunde in größeren Haltungen, Jungtiere, Hunde mit Kontakt zu anderen Tieren, Jagdhunde, Streuner und Tiere, die mit rohen Fleischprodukten gefüttert werden, besteht ein höheres Infektionsrisiko.
Gefahren für den Menschen
Der Mensch ist für den Hundespulwurm Toxocara canis und den Hundehakenwurm (Ancylostoma caninum) ein Fehlwirt, das heißt, die Larven schädigen befallene Organe, aber es findet keine Entwicklung zu adulten Würmern statt.
Beide sind in Mitteleuropa die wichtigsten Zoonoseerreger unter den Fadenwürmern des Hundes.
Fadenwürmer besiedeln als sogenannte „Innenschmarotzer“ verschiedene innere Organe – die meisten von ihnen den Verdauungstrakt – und die Haut. Bislang sind bei Hunden etwa 30 verschiedene Fadenwurmarten nachgewiesen worden; sie sind im Wesentlichen auch bei wildlebenden Hundearten zu finden. Die Mehrzahl davon ruft aber bei erwachsenen Tieren häufig keine oder nur geringe Krankheitserscheinungen hervor.
Die Infektion muss sich also nicht zwangsläufig auch in einer Wurmerkrankung äußern. Für die meisten Fadenwürmer lässt sich eine Infektion durch eine Untersuchung des Kots auf Eier oder Larven nachweisen. Von gesundheitspolitischer Bedeutung ist in Mitteleuropa vor allem der Befall mit dem Hundespulwurm und dem Hundehakenwurm, da sie auch auf den Menschen übergehen können (Zoonose).
Eine regelmäßige Entwurmung kann die Befallshäufigkeit und damit die Infektionsgefahr für Menschen und Hunde deutlich reduzieren.
Parasitosen des Verdauungstrakts
Spulwurmbefall
Bei Hunden treten zwei Spulwurmarten auf: Toxocara canis und Toxascaris leonina.
Während die Infektion mit T. leonina nur sehr selten klinische Erscheinungen wie Durchfall hervorruft, ist die krankheitsauslösende Wirkung von T. canis deutlich stärker.
Bei Welpen treten ein herabgesetztes Allgemeinbefinden, struppiges Fell, Zurückbleiben im Wachstum, abwechselnd Durchfall und Verstopfung, ein aufgetriebener Bauch („Wurmbauch“) und Blutarmut auf. Komplikationen des T.-canis-Befalls mit teilweise tödlichem Ausgang sind Darmverschluss durch Wurmknäuel, Dünndarmdurchbruch, Lungenentzündung, Leberentzündung oder neurologische Erscheinungen durch verirrte Wanderlarven im Zentralnervensystem.
Die Diagnose kann bei Würmern in Erbrochenem bereits ohne Spezialuntersuchungen gestellt werden. Relativ sicher kann ein Spulwurmbefall durch den mikroskopischen Nachweis der über das Flotationsverfahren aus dem Kot herausgelösten Eier nachgewiesen werden, allerdings erst nach Ablauf der Präpatenz.
Hakenwurmbefall (Ankylostomyasis)
Bei Hunden kommen vor allem zwei Hakenwurmarten vor: Ancylostoma caninum und Uncinaria stenocephala. Sie parasitieren im Dünndarm und verursachen durch das Saugen von Blut eine Blutarmut sowie Schädigungen der Darmschleimhaut.
Die Würmer haben mit etwa 5–15 mm nur etwa ein Zehntel der Länge von Spulwürmern, ein hakenförmig abgewinkeltes Vorderende (daher der Name „Hakenwurm“) und eine große Mundkapsel mit Schneidplatten.
Während der Befall mit U. stenocephala häufig nur geringe Krankheitserscheinungen wie Durchfall verursacht, kann der Befall mit A. caninum vor allem bei Welpen schwere Krankheitsbilder verursachen. Dabei können blutiger Durchfall, starke Abgeschlagenheit und Blutarmut auftreten, teilweise mit akutem oder perakuten Verlauf und plötzlichen Todesfällen.
Bei chronischem Verlauf bleiben die Jungtiere im Wachstum zurück, sind teilnahmslos, zeigen mangelnden Appetit, Durchfall und Abmagerung. Eher selten tritt eine Lungenentzündung durch wandernde Larven auf. Ein Hakenwurmbefall kann durch den Nachweis der Eier im Kot mittels Flotationsverfahren diagnostiziert werden.
Peitschenwurmbefall (Trichuriasis)
Die krankheitsauslösende Wirkung von T. vulpis ist mittelgradig. Befallene Hunde zeigen Durchfall, der blutig, bei weniger schwerem Verlauf mit Schleim durchsetzt ist. Die Tiere magern ab, Jungtiere bleiben im Wachstum zurück, bei starkem Befall kann sich eine Blutarmut entwickeln. Eine sichere Diagnose kann nur über den Einachweis im Kot mittels Flotationsverfahren gestellt werden.
Zwergfadenwurmbefall (Strongyloidiasis)
Die Infektion mit dem Zwergfadenwurm Strongyloides canis kann durch Aufnahme infektiöser Larven über die Muttermilch, perorale Aufnahme oder durch aktives Eindringen der Larven durch die Haut erfolgen. Eine Autoinfektion, also die Infektion des gleichen Tieres durch von ihm ausgeschiedene Larven, ist möglich. S. canis parasitiert im Dünndarm. Die Eier sind etwa 50 µm lang und enthalten bei Ausscheidung mit dem Kot bereits die infektiöse Larve.
Die Strongyloidiasis verursacht bei Welpen akuten bis chronischen Durchfall, gelegentlich auch eine Verstopfung. Die Diagnose kann durch den Nachweis der Eier im Kot mittels Flotationsverfahren gestellt werden.
Magenwurmbefall
Magenwürmer gehören zu einer weltweit verbreiteten Gattung von Fadenwürmern, welche die Schleimhaut von Magen und Zwölffingerdarm befallen können.
Die Magenwürmer verursachen Schäden an der Magenschleimhaut, was zu Gastritis, Blutungen und chronischem Erbrechen führt.
Bei starkem Befall kommt es zu Gewichtsverlust und Blutarmut. Der Nachweis der Eier im Kot mit dem Flotationsverfahren ist unsicher, da sie kaum aufschwemmen. Daher gibt es keine systematischen Untersuchungen zur Vorkommenshäufigkeit. Eine sichere Diagnose kann mittels Magenspülproben oder einer Magenspiegelung gestellt werden.
Speiseröhrenwurmbefall
Die Würmer können während ihrer Wanderung gelegentlich ein Aortenaneurysma verursachen, oft sind befallene Hunde jedoch symptomlos. In der Speiseröhre selbst verursacht S. lupi eine granulomatöse Gewebsreaktion, welche ohne Behandlung sehr oft entartet und dann verschiedene bösartige Tumoren bildet.
Durch die tumorbedingte Raumforderung im Brustkorb kann es zusätzlich auch zu einer hypertrophischen Osteopathie kommen.
Parasitosen der Atemwege
Lungenhaarwurmbefall (Capillariasis)
Der Lungenwurm Crenosoma vulpis ist bis zu 1,6 cm lang und wird indirekt über das Fressen von Zwischenwirten wie Schnecken übertragen. Klinisch ist eine Infektion durch chronischen Husten gekennzeichnet und ähnelt einer allergischen Bronchitis. Der Nachweis von C. vulpis in Kotproben mit Standardflotationsverfahren ist relativ unsicher.
Filaroididae
Kommt beim Hund relativ selten vor. Das gleichzeitige Auftreten ähnlicher Symptome bei der Mutter und ihrer Welpen ist ein Hinweis auf eine solche Infektion. Gelegentlich kann bei Belastung eine anfallsartige Atemnot auftreten. Fieber tritt zumeist nicht auf.
Zur Diagnose kann der Nachweis von Knötchen mittels Lungenspiegelung, eventuell auch auf Röntgenbildern des Brustkorbs, sowie der Larven in Lungenspülflüssigkeit oder Luftröhrenabstrichen genutzt werden. Der Nachweis von Larven im Kot mittels Flotationsverfahren ist unsicher, zumal die Larven nur unregelmäßig über den Kot ausgeschieden werden, während der relativ langen Präpatenz überhaupt nicht.
Parasitosen des Blutkreislaufs
Herzwurmbefall (Dirofilariose)
Befallene Tiere zeigen mit der Entwicklung der reifen Würmer, also erst etwa sechs Monate nach der Infektion, eine reduzierte Leistungsfähigkeit und ermüden schnell. Es entwickelt sich eine Rechtsherzinsuffizienz mit Überlastung und Erweiterung der rechten Herzseite, die sich in Atemnot, Husten und der Bildung von Ödemen äußert. Infolge der Herzinsuffizienz kann auch ein Leber- und Nierenversagen entstehen.
Angiostrongylose
Der französische Herzwurm (Angiostrongylus vasorum) ist ein Parasit des Lungengefäßstamms, der Lungenarterien und der rechten Herzkammer. Klinisch zeigen befallene Hunde eine langsam fortschreitende Einschränkung der Herz- und/oder Lungenfunktion. Chronischer Husten, Atemnot, Nahrungsverweigerung und Gewichtsabnahme sind ebenfalls häufige Symptome.
Riesennierenwurmbefall
Der Riesennierenwurm ist der größte bekannte parasitische Fadenwurm und kann beim Hund die Niere, gelegentlich auch die Bauchhöhle befallen. Weibliche Würmer erreichen Längen von über einem Meter bei einem Durchmesser von bis zu 12 mm; männliche Würmer messen 20 cm auf 6–8 mm. Beide Geschlechter haben eine blutrote Farbe.
Bei Hunden verbleibt der Parasit allerdings recht häufig in der Bauchhöhle, was für den Hund weniger gravierende Folgen hat als ein Befall der Niere. Die befallene Niere wird durch den Parasiten langsam zerstört, der dabei üblicherweise auch das Nierenbecken perforiert. Da Eier im Urin sehr selten auftreten, ist deren Nachweis zur Diagnostik ungeeignet. Ein Nierenwurmbefall kann mittels Sonografie nachgewiesen werden.
Harnblasenhaarwurmbefall
Der Harnblasenhaarwurm ist 13 bis 60 mm lang und besiedelt die Harnblase, gelegentlich auch den Harnleiter und das Nierenbecken.
Bei Hunden in größeren Zwingern können bis zu drei Viertel der Tiere befallen sein. C. plica ruft selten Krankheitserscheinungen hervor. Bei stärkerem Befall kann es zu einer Harnblasenentzündung mit Harndrang und Harninkontinenz kommen. Die Diagnose kann durch den Einachweis im Urin gestellt werden, allerdings aufgrund der langen Präpatenz nicht bei Tieren, die jünger als acht Monate sind.
Parasitosen der Haut
Peloderose
Die Läsionen sind normalerweise auf diejenigen Hautteile beschränkt, die in direktem Kontakt mit dem infektiösen Material waren, meistens also Bauch, Unterbrust und Extremitäten. Die betroffene Haut ist gerötet, mäßig bis stark entzündet und teilweise bis völlig haarlos. Es besteht ein ausgeprägter Juckreiz, der zu weiteren Hautläsionen (Krustenbildung) und bakteriellen Sekundärinfektionen führen kann. Normalerweise ist die Krankheit selbstlimitierend, auch weil der Hund für die Würmer einen Fehlwirt darstellt.
Kutane Dirofilariose
Dirofilaria repens ist ein Parasit des Unterhautgewebes bei Hunden. Als Zwischenwirt und Überträger fungieren Stechmücken. Er kommt vor allem in Süd-, südlichem Ost- und Westeuropa sowie weiten Teilen Asiens vor, breitet sich aber immer weiter nach Nordeuropa aus und wird auch in Deutschland zunehmend nachgewiesen.
Der Befall mit D. repens verursacht gelegentlich Hautknoten, Schwellungen, Juckreiz, Abszesse und Haarausfall, verläuft aber oft auch völlig ohne klinische Symptome.
Thelaziose
Die Thelaziose wird durch Vertreter der Gattung Thelazia hervorgerufen. Es handelt sich um weißliche Fadenwürmer von etwa 1,5 cm Länge, in Deutschland eher selten. Thelazien parasitieren am Augapfel unter der Nickhaut sowie in den Tränenwegen und verursachen eine Bindehautentzündung und vermehrten Tränenfluss.
Auch eine Verlegung der Tränenwege oder eine Hornhautentzündung kann auftreten. Bei starkem Befall sind die Würmer bereits mit bloßem Auge sichtbar. Eine sichere Diagnose kann durch den Nachweis der Würmer oder ihrer Larven in Augenspülproben oder einem Bioptat der Tränendrüse erfolgen.
Onchozerkose
Erreger der Onchozerkose der Hunde ist Onchocerca lupi. Die Erkrankung kommt in Nordamerika und einigen Ländern Europas (Griechenland, Ungarn) vor, ist aber selten.
Die Würmer rufen erbsen- bis bohnengroße granulomatöse Knötchen in der Sclera, der Augenumgebung und Bindehaut hervor. Unter Umständen kann sich eine lymphoplasmazytäre Entzündung der mittleren Augenhaut entwickeln. Die Diagnose kann durch den Nachweis der Würmer in den Knötchen gestellt werden.
Bekämpfung
Die meisten Infektionen sind für erwachsene Hunde eher harmlos, da sich bei intaktem Immunsystem ein Erreger-Wirt-Gleichgewicht einstellt. Da aber einige von ihnen gesundheitliche Störungen auslösen können und einige auch eine potentielle Gefahr für den Menschen darstellen, sind regelmäßige Wurmkuren bei Hunden durchaus sinnvoll. Vor allem für Hunde in größeren Haltungen, Jungtiere, Hunde mit Kontakt zu anderen Tieren, Jagdhunde, Streuner und Tiere, die mit rohen Fleischprodukten gefüttert werden, besteht ein höheres Infektionsrisiko.
Gefahren für den Menschen
Der Mensch ist für den Hundespulwurm Toxocara canis und den Hundehakenwurm (Ancylostoma caninum) ein Fehlwirt, das heißt, die Larven schädigen befallene Organe, aber es findet keine Entwicklung zu adulten Würmern statt.
Beide sind in Mitteleuropa die wichtigsten Zoonoseerreger unter den Fadenwürmern des Hundes.
eingestellt von: ise; Quellen- und Bildnachweis
Giardiose des Hundes
Die Giardiose des Hundes (Syn. Giardiasis, Lambliasis) ist eine durch den Einzeller Giardia intestinalis hervorgerufene häufige Durchfallerkrankung bei Hunden. Beim Hund herrschen die hundespezifischen Genotypen D und C des Parasiten vor. Etwa 20 % der Erkrankungen bei Hunden werden jedoch durch den Genotyp A ausgelöst, der auch für die Giardiasis des Menschen verantwortlich ist. Diese Erkrankungen sind damit als Zoonose einzustufen. Betroffen sind vor allem Welpen, Junghunde und Hunde in größeren Gruppen wie Zuchten oder Tierheimen.
Die Erkrankung zeigt sich in immer wiederkehrenden Durchfällen mit einem gelblichen, dünnbreiigen und faulig stinkenden Kot. Zur Bekämpfung werden gegen Einzeller wirksame Antiparasitika eingesetzt, die medikamentöse Behandlung muss aber durch eine konsequente Umgebungsbehandlung ergänzt werden.
Klinisches Bild
Das klinische Bild variiert in Abhängigkeit vom Infektionsabwehrvermögen des Hundes und der krankheitsauslösenden Wirkung des beteiligten Giardienstamms. Unter Umständen bleibt die Infektion stumm, also ohne sichtbare klinische Symptome.
Erkrankte Hunde zeigen immer wieder auftretende Durchfälle, Fettkot, Malabsorption mit verringerter Gewichtszunahme beziehungsweise Abmagerung sowie Appetitlosigkeit. Der Kot ist zumeist weich und ungeformt, gelblich und faulig oder ranzig riechend. Gelegentlich kann er auch schleimig oder wässrig sein, als Zeichen der Malabsorption mit Gasblasen durchsetzt sein oder auch geringe Blutbeimengungen zeigen.
Bekämpfung
Zur Behandlung der Giardiose werden Fenbendazol, Metronidazol oder Febantel eingesetzt, wobei Fenbendazol als Mittel der Wahl gilt.
Werden mehrere Tiere gehalten, müssen sie mitbehandelt werden, auch wenn sie keine klinischen Symptome zeigen. Metronidazol hat auch einen Effekt auf die bakterielle Darmflora, so dass auch eine Kombination mit Fenbendazol sinnvoll sein kann. Bei Therapieversagern kann auch Albendazol Anwendung finden.
Wichtig ist die konsequente Umgebungsbehandlung und Verhinderung der Umweltkontamination, um Reinfektionen oder Infektionen anderer Tiere oder des Menschen zu verhindern. Der Kot sollte täglich entfernt und in Plastiktüten über den Hausmüll entsorgt werden. Da der Giardiengenotyp A auch für den Menschen krankheitsauslösend ist, sollten infizierte Hunde von Spielplätzen und Sandkästen ferngehalten werden, eine Maßnahme, die auch zum Schutz von Kindern vor Hundespul- und Bandwürmern eigentlich selbstverständlich sein sollte.
Auslaufflächen werden mit einem Dampfstrahler mit über 60 °C gereinigt und anschließend abtrocknen gelassen, feuchte Areale sollten trockengelegt werden. Gegenstände wie Spielzeug, Futter- und Trinknäpfe müssen täglich mit kochendem Wasser übergossen und anschließend gründlich abgetrocknet, Liegedecken so heiß wie möglich gewaschen werden. Wenn möglich, sollten Futter- und Trinkgefäße vor Fliegen geschützt werden, da diese Giardien weiterverbreiten können. Zudem sollte das Fell befallener Hunde zu Beginn täglich shampooniert werden um die Zahl anhaftender Zysten zu reduzieren.
Die Erkrankung zeigt sich in immer wiederkehrenden Durchfällen mit einem gelblichen, dünnbreiigen und faulig stinkenden Kot. Zur Bekämpfung werden gegen Einzeller wirksame Antiparasitika eingesetzt, die medikamentöse Behandlung muss aber durch eine konsequente Umgebungsbehandlung ergänzt werden.
Klinisches Bild
Das klinische Bild variiert in Abhängigkeit vom Infektionsabwehrvermögen des Hundes und der krankheitsauslösenden Wirkung des beteiligten Giardienstamms. Unter Umständen bleibt die Infektion stumm, also ohne sichtbare klinische Symptome.
Erkrankte Hunde zeigen immer wieder auftretende Durchfälle, Fettkot, Malabsorption mit verringerter Gewichtszunahme beziehungsweise Abmagerung sowie Appetitlosigkeit. Der Kot ist zumeist weich und ungeformt, gelblich und faulig oder ranzig riechend. Gelegentlich kann er auch schleimig oder wässrig sein, als Zeichen der Malabsorption mit Gasblasen durchsetzt sein oder auch geringe Blutbeimengungen zeigen.
Bekämpfung
Zur Behandlung der Giardiose werden Fenbendazol, Metronidazol oder Febantel eingesetzt, wobei Fenbendazol als Mittel der Wahl gilt.
Werden mehrere Tiere gehalten, müssen sie mitbehandelt werden, auch wenn sie keine klinischen Symptome zeigen. Metronidazol hat auch einen Effekt auf die bakterielle Darmflora, so dass auch eine Kombination mit Fenbendazol sinnvoll sein kann. Bei Therapieversagern kann auch Albendazol Anwendung finden.
Wichtig ist die konsequente Umgebungsbehandlung und Verhinderung der Umweltkontamination, um Reinfektionen oder Infektionen anderer Tiere oder des Menschen zu verhindern. Der Kot sollte täglich entfernt und in Plastiktüten über den Hausmüll entsorgt werden. Da der Giardiengenotyp A auch für den Menschen krankheitsauslösend ist, sollten infizierte Hunde von Spielplätzen und Sandkästen ferngehalten werden, eine Maßnahme, die auch zum Schutz von Kindern vor Hundespul- und Bandwürmern eigentlich selbstverständlich sein sollte.
Auslaufflächen werden mit einem Dampfstrahler mit über 60 °C gereinigt und anschließend abtrocknen gelassen, feuchte Areale sollten trockengelegt werden. Gegenstände wie Spielzeug, Futter- und Trinknäpfe müssen täglich mit kochendem Wasser übergossen und anschließend gründlich abgetrocknet, Liegedecken so heiß wie möglich gewaschen werden. Wenn möglich, sollten Futter- und Trinkgefäße vor Fliegen geschützt werden, da diese Giardien weiterverbreiten können. Zudem sollte das Fell befallener Hunde zu Beginn täglich shampooniert werden um die Zahl anhaftender Zysten zu reduzieren.
eingestellt von: ise; Quellennachweis
Hepatozoonose
Die Hepatozoonose ist eine durch parasitäre Einzeller der Gattung Hepatozoon hervorgerufene Krankheit bei Hunden. Sie verläuft unspezifisch mit Fieber, Gewichtsverlust und Schmerzen in der Lendenregion. Gelegentlich treten blutige Durchfälle auf. Eine vollständige Heilung ist nicht möglich, die Erkrankung ist mit Antiprotozoika jedoch unter Kontrolle zu bringen. Die wirksamste Vorbeugung ist der Schutz vor Zecken, über deren orale Aufnahme die Infektion erfolgt.
Erreger und Übertragung
In Europa, Afrika und Asien wird die Hepatozoonose vor allem durch Hepatozoon canis hervorgerufen. Der Erreger kommt in Südeuropa, Afrika und Asien vor, so dass die Hepatozoonose in Mitteleuropa vor allem eine „Reisekrankheit“ ist.
In den Sommermonaten kann die Braune Hundezecke aber auch in Mitteleuropa vorkommen, in beheizten Räumen auch ganzjährig, so dass auch ein Infektionsrisiko auch hier besteht.
Der Erreger wird oral durch Fressen, Verschlucken oder Zerbeißen der Zecken übertragen. Empfänglich sind vor allem Hunde. Hepatozoen befallen die weißen Blutkörperchen, insbesondere die eosinophilen Granulozyten und Monozyten, sowie Endothelzellen der Milz, Leber, Muskulatur, Lungen und des Knochenmarks. In Geweben verursacht die Infektion eine eitrig-granulomatöse Entzündung. Durch Bildung von Immunkomplexen kann eine Glomerulonephritis oder Amyloidose entstehen.
Klinisches Bild
Die Inkubationszeit beträgt zwei bis vier Wochen. Das klinische Bild ist unspezifisch. Zeichen der Allgemeininfektion sind Fieberschübe, Gewichtsabnahme und Lymphknotenschwellungen. Die Schleimhäute können aufgrund einer Anämie blass erscheinen.
Durch Eindringen der Sporozoiten in die Darmschleimhaut kann es zu blutigen Durchfällen und Inappetenz kommen. Bei Schizontenbildung in der Muskulatur treten Überempfindlichkeit vor allem in der Lendenregion, Muskelentzündungen, steifer Gang und Muskelschwund auf. Bei jungen Hunden kommt es häufig zu einer Reaktion der Knochen mit Ausnahme des Schädels.
Behandlung
Eine vollständige Elimination des Erreger ist nicht möglich. Eine klinische Heilung kann mit einer Kombination aus Imidocarb und Doxycyclin oder mit Trimethoprim und Sulfonamiden erreicht werden. Gegen Hepatozoon americanum ist eine Kombination aus Trimethoprim, Sulfadiazin, Pyrimethamin und Clindamycin wirksam.
Decoquinat vermindert die Gefahr von Rezidiven und erhöht die Überlebenszeit.
Eine Prophylaxe ist vor allem durch Verhinderung eines Zeckenbefalls möglich. Milbenabweisende und -abtötende Wirkungen haben Amitraz, Fipronil, Permethrin, Propoxur und Pyriprol, die bei Auftropfen auf die Haut (pour on) eine Schutzwirkung von etwa vier Wochen haben. Deltamethrin und Propoxur haben bei Anwendung in Form imprägnierter Halsbänder eine Schutzwirkung von etwa sechs, Dimpylat von vier Monaten.
Erreger und Übertragung
In Europa, Afrika und Asien wird die Hepatozoonose vor allem durch Hepatozoon canis hervorgerufen. Der Erreger kommt in Südeuropa, Afrika und Asien vor, so dass die Hepatozoonose in Mitteleuropa vor allem eine „Reisekrankheit“ ist.
In den Sommermonaten kann die Braune Hundezecke aber auch in Mitteleuropa vorkommen, in beheizten Räumen auch ganzjährig, so dass auch ein Infektionsrisiko auch hier besteht.
Der Erreger wird oral durch Fressen, Verschlucken oder Zerbeißen der Zecken übertragen. Empfänglich sind vor allem Hunde. Hepatozoen befallen die weißen Blutkörperchen, insbesondere die eosinophilen Granulozyten und Monozyten, sowie Endothelzellen der Milz, Leber, Muskulatur, Lungen und des Knochenmarks. In Geweben verursacht die Infektion eine eitrig-granulomatöse Entzündung. Durch Bildung von Immunkomplexen kann eine Glomerulonephritis oder Amyloidose entstehen.
Klinisches Bild
Die Inkubationszeit beträgt zwei bis vier Wochen. Das klinische Bild ist unspezifisch. Zeichen der Allgemeininfektion sind Fieberschübe, Gewichtsabnahme und Lymphknotenschwellungen. Die Schleimhäute können aufgrund einer Anämie blass erscheinen.
Durch Eindringen der Sporozoiten in die Darmschleimhaut kann es zu blutigen Durchfällen und Inappetenz kommen. Bei Schizontenbildung in der Muskulatur treten Überempfindlichkeit vor allem in der Lendenregion, Muskelentzündungen, steifer Gang und Muskelschwund auf. Bei jungen Hunden kommt es häufig zu einer Reaktion der Knochen mit Ausnahme des Schädels.
Behandlung
Eine vollständige Elimination des Erreger ist nicht möglich. Eine klinische Heilung kann mit einer Kombination aus Imidocarb und Doxycyclin oder mit Trimethoprim und Sulfonamiden erreicht werden. Gegen Hepatozoon americanum ist eine Kombination aus Trimethoprim, Sulfadiazin, Pyrimethamin und Clindamycin wirksam.
Decoquinat vermindert die Gefahr von Rezidiven und erhöht die Überlebenszeit.
Eine Prophylaxe ist vor allem durch Verhinderung eines Zeckenbefalls möglich. Milbenabweisende und -abtötende Wirkungen haben Amitraz, Fipronil, Permethrin, Propoxur und Pyriprol, die bei Auftropfen auf die Haut (pour on) eine Schutzwirkung von etwa vier Wochen haben. Deltamethrin und Propoxur haben bei Anwendung in Form imprägnierter Halsbänder eine Schutzwirkung von etwa sechs, Dimpylat von vier Monaten.
eingestellt von: ise; Quellennachweis
Herzwurmerkrankung
Die Herzwurmerkrankung (kardiovaskuläre Dirofilariose) ist eine parasitäre Krankheit der Hunde. Sie ist nur schwer zu behandeln und verläuft oft tödlich. Sie kommt vor allem in Nord- und Mittelamerika vor, ist aber auch im Mittelmeerraum (vor allem in Italien, Griechenland, Südfrankreich, Portugal und auf den Kanarischen Inseln) und den tropischen und subtropischen Gebieten verbreitet. Einzelfälle wurden auch in Ungarn und im Tessin beobachtet, weshalb insbesondere Hunde bei Urlaubsreisen in diese Regionen ansteckungsgefährdet sind.
Erreger
Der Erreger der Dirofilariose ist die Filarienart Dirofilaria immitis. Diese Parasiten sind obligat zweiwirtig. Ein Teil des Entwicklungszyklus, vom Larvenstadium 1 bis 3 verläuft in Stechmücken. Bislang wurden über 70 Stechmückenarten als Träger nachgewiesen, allerdings nicht die in Mitteleuropa heimischen Arten.
Die Stechmücke überträgt beim Saugakt diese Mikrofilarien auf den Wirt. In der Unterhaut erfolgt innerhalb von 2 Monaten die Entwicklung zum Larvenstadium 4. Diese Larven 4 wandern über die Muskulatur in die Blutgefäße ein und entwickeln sich nach weiteren zwei bis drei Monaten zu den erwachsenen Herzwürmern (Makrofilarien).
Die erwachsenen Herzwürmer sind etwa 1 mm dick und 20 bis 30 cm lang und siedeln sich vor allem im Truncus pulmonalis, bei stärkerem Befall auch in der rechten Herzhälfte und den herznahen Abschnitten der Hohlvenen an. Etwa sechs Monate nach der Infektion bilden die Weibchen wiederum Mikrofilarien (Larve 1), die mit dem Blut in kleinere Blutgefäße gelangen und gegebenenfalls von Mücken beim Saugakt wieder aufgenommen werden. Mikrofilarien können bis zu drei Jahre in der Blutbahn zirkulieren.
Die Erkrankung kommt in den endemischen Gebieten vor allem beim Hund vor. Katzen sind deutlich seltener betroffen, die Prävalenz ist nur etwa 10 % der bei Hunden. Auch Füchse, Robben und selten auch Menschen können erkranken.
Die Infektion mit der verwandten Art Dirofilaria repens bleibt auf die Haut beschränkt und ruft nur selten klinische Symptome hervor.
Therapie
Die Therapie ist kompliziert, da Herzwürmer zwar für Wirkstoffe wie Diethylcarbamazin oder Melarsamin prinzipiell empfänglich sind, aber bei stärkerem Befall eine Embolie oder eine schwere anaphylaktische Reaktion infolge des massiven Absterbens von Mikrofilarien entstehen kann. Die Behandlung wird deshalb meist mit Acetylsalicylsäure und bei schwerem Befall mit Antihistaminika kombiniert. Die Behandlung mit Levamisol kann bei Hunden ebenfalls schwere Nebenwirkungen (Blutungen, hämolytische Anämie) hervorrufen. Die operative Entfernung der Herzwürmer ist ebenfalls risikobehaftet und nur in spezialisierten Kliniken möglich.
Wegen der Probleme bei der Therapie ist die Vorbeugung umso wichtiger. Eine Behandlung mit Ivermectin, Moxidectin, Selamectin, Milbemycinoxim oder Lufenuron vor Beginn der Urlaubsreise kann eine Infektion verhindern.
Zudem sollten Maßnahmen ergriffen werden, um die Exposition von Hunden gegenüber Mücken zu minimieren.
Erreger
Der Erreger der Dirofilariose ist die Filarienart Dirofilaria immitis. Diese Parasiten sind obligat zweiwirtig. Ein Teil des Entwicklungszyklus, vom Larvenstadium 1 bis 3 verläuft in Stechmücken. Bislang wurden über 70 Stechmückenarten als Träger nachgewiesen, allerdings nicht die in Mitteleuropa heimischen Arten.
Die Stechmücke überträgt beim Saugakt diese Mikrofilarien auf den Wirt. In der Unterhaut erfolgt innerhalb von 2 Monaten die Entwicklung zum Larvenstadium 4. Diese Larven 4 wandern über die Muskulatur in die Blutgefäße ein und entwickeln sich nach weiteren zwei bis drei Monaten zu den erwachsenen Herzwürmern (Makrofilarien).
Die erwachsenen Herzwürmer sind etwa 1 mm dick und 20 bis 30 cm lang und siedeln sich vor allem im Truncus pulmonalis, bei stärkerem Befall auch in der rechten Herzhälfte und den herznahen Abschnitten der Hohlvenen an. Etwa sechs Monate nach der Infektion bilden die Weibchen wiederum Mikrofilarien (Larve 1), die mit dem Blut in kleinere Blutgefäße gelangen und gegebenenfalls von Mücken beim Saugakt wieder aufgenommen werden. Mikrofilarien können bis zu drei Jahre in der Blutbahn zirkulieren.
Die Erkrankung kommt in den endemischen Gebieten vor allem beim Hund vor. Katzen sind deutlich seltener betroffen, die Prävalenz ist nur etwa 10 % der bei Hunden. Auch Füchse, Robben und selten auch Menschen können erkranken.
Die Infektion mit der verwandten Art Dirofilaria repens bleibt auf die Haut beschränkt und ruft nur selten klinische Symptome hervor.
Therapie
Die Therapie ist kompliziert, da Herzwürmer zwar für Wirkstoffe wie Diethylcarbamazin oder Melarsamin prinzipiell empfänglich sind, aber bei stärkerem Befall eine Embolie oder eine schwere anaphylaktische Reaktion infolge des massiven Absterbens von Mikrofilarien entstehen kann. Die Behandlung wird deshalb meist mit Acetylsalicylsäure und bei schwerem Befall mit Antihistaminika kombiniert. Die Behandlung mit Levamisol kann bei Hunden ebenfalls schwere Nebenwirkungen (Blutungen, hämolytische Anämie) hervorrufen. Die operative Entfernung der Herzwürmer ist ebenfalls risikobehaftet und nur in spezialisierten Kliniken möglich.
Wegen der Probleme bei der Therapie ist die Vorbeugung umso wichtiger. Eine Behandlung mit Ivermectin, Moxidectin, Selamectin, Milbemycinoxim oder Lufenuron vor Beginn der Urlaubsreise kann eine Infektion verhindern.
Zudem sollten Maßnahmen ergriffen werden, um die Exposition von Hunden gegenüber Mücken zu minimieren.
eingestellt von: ise; Quellen- und Bildnachweis
x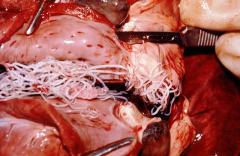

Quellen- und Bildnachweis

Bildname:
Mit Herzwurm infiziertes Hundeherz
Urheber:
Wikipedia/Alan Walker R
Link:
Kokzidiose der Hunde
Die Kokzidiose der Hunde ist eine parasitologische Erkrankung der Hunde, die mit Durchfall einhergeht. Sie wird durch verschiedene Einzeller aus der Gattung Cystoisospora verursacht. Klinische Symptome zeigen vor allem Welpen und Junghunde. Die Behandlung erfolgt durch kokzidienwirksame Antibiotika bzw. Antiprotozoika.
Ursache und Vorkommen
Für Hunde sind vor allem Cystoisospora canis, C. ohiosensis und C. burrowsi krankheitsauslösend, wobei C. canis die höchste Pathogenität aufweist und häufig Mischinfektionen auftreten.Andere Tierarten sind aufgrund der Wirtsspezifität des Erregers nicht gefährdet.
Bei Hunden in Deutschland wurde eine Prävalenz von 8–16 % ermittelt, wobei Junghunde die höchsten Befallsraten aufwiesen.Die Erkrankung tritt vor allem in größeren Zuchten auf, wobei symptomlose erwachsene Hunde als Ausscheider fungieren. Die Ansteckung erfolgt als Schmutzinfektion mit sporulierten Oozysten. Die Kokzidien entwickeln sich in den Epithelzellen des Dünn- und Dickdarms.
Sechs bis zwölf Tage nach der Infektion werden wiederum für bis zu elf Tage Oozysten ausgeschieden, die nach zwei bis vier Tagen in der Außenwelt ansteckungsfähig sind.
Klinik und Behandlung
Klinische Erscheinungen treten vor allem bei Welpen und Junghunden auf. Sie zeigen sich in dünnbreiigem, selten auch wässrig-blutigen Durchfall. Unter Umständen können sich Allgemeinstörungen wie Appetitlosigkeit, Abmagerung, Dehydratation und Fieber einstellen.
Bei schweren Verläufen können auch Todesfälle auftreten. Die Krankheitserscheinungen können selbst innerhalb eines Wurfes sehr stark variieren. Erwachsene Tiere erkranken nur bei Störungen des Immunsystems. Die Diagnose wird durch den Nachweis der Oozysten im Kot mittels Flotationsverfahren gestellt. Bei erkrankten Tieren lassen sich im Kot meist deutlich mehr Kokzidienoozysten nachweisen als bei inapparent infizierten.
Reinigungs- und Desinfektionmaßnahmen mit kokzidienwirksamen Mitteln sind für eine Eliminierung der Krankheit aus Zwingern unumgänglich
Ursache und Vorkommen
Für Hunde sind vor allem Cystoisospora canis, C. ohiosensis und C. burrowsi krankheitsauslösend, wobei C. canis die höchste Pathogenität aufweist und häufig Mischinfektionen auftreten.Andere Tierarten sind aufgrund der Wirtsspezifität des Erregers nicht gefährdet.
Bei Hunden in Deutschland wurde eine Prävalenz von 8–16 % ermittelt, wobei Junghunde die höchsten Befallsraten aufwiesen.Die Erkrankung tritt vor allem in größeren Zuchten auf, wobei symptomlose erwachsene Hunde als Ausscheider fungieren. Die Ansteckung erfolgt als Schmutzinfektion mit sporulierten Oozysten. Die Kokzidien entwickeln sich in den Epithelzellen des Dünn- und Dickdarms.
Sechs bis zwölf Tage nach der Infektion werden wiederum für bis zu elf Tage Oozysten ausgeschieden, die nach zwei bis vier Tagen in der Außenwelt ansteckungsfähig sind.
Klinik und Behandlung
Klinische Erscheinungen treten vor allem bei Welpen und Junghunden auf. Sie zeigen sich in dünnbreiigem, selten auch wässrig-blutigen Durchfall. Unter Umständen können sich Allgemeinstörungen wie Appetitlosigkeit, Abmagerung, Dehydratation und Fieber einstellen.
Bei schweren Verläufen können auch Todesfälle auftreten. Die Krankheitserscheinungen können selbst innerhalb eines Wurfes sehr stark variieren. Erwachsene Tiere erkranken nur bei Störungen des Immunsystems. Die Diagnose wird durch den Nachweis der Oozysten im Kot mittels Flotationsverfahren gestellt. Bei erkrankten Tieren lassen sich im Kot meist deutlich mehr Kokzidienoozysten nachweisen als bei inapparent infizierten.
Reinigungs- und Desinfektionmaßnahmen mit kokzidienwirksamen Mitteln sind für eine Eliminierung der Krankheit aus Zwingern unumgänglich
eingestellt von: ise; Quellennachweis
Leishmaniose
Eine Leishmaniose ist eine weltweit bei Mensch und Tier vorkommende Infektionserkrankung, die durch obligat intrazelluläre protozoische Parasiten der Gattung Leishmania hervorgerufen wird. Das Verbreitungsgebiet sind die Tropen, besonders Peru, Kolumbien und das östliche Afrika, aber auch der Mittelmeerraum und Asien.
Übertragung
Die Übertragung erfolgt durch Sandmücken (aus der Familie der Schmetterlingsmücken). In den 1950er Jahren wurden durch den Einsatz von Insektiziden (hauptsächlich DDT) gegen Malaria-übertragende Anophelesmücken auch die Sandmücken (Phlebotominae) stark dezimiert. Heute haben sich die Sandmückenpopulationen wieder auf das ursprüngliche Niveau vermehrt, wodurch im Mittelmeerraum die Erkrankungszahlen an Leishmaniosen bei Mensch und Tier wieder zunehmen.
Die Leishmaniose-Infektionsrate von Hunden ist besonders im Mittelmeerraum stellenweise sehr hoch: In Andalusien sind bis zu 42 % der Hunde infiziert, auf Sizilien bis zu 80 %. Die Infektionsrate bei Menschen und Hunden hängt von der lokalen Sandmückenpopulation, deren Durchseuchung und Stechgewohnheiten ab.
Klinik, Diagnostik
Infolge der Tatsache, dass Leishmanien nahezu alle Organsysteme des Körpers befallen können, kann sich die Krankheit sehr vielfältig darstellen. Einem Großteil der erkrankten Tiere ist jedoch das Auftreten von Störungen der Haut gemein. Anhand der Verteilung dieser Störung können Rückschlüsse auf die Prognose der Erkrankung gezogen werden:
- symmetrischer Haarverlust und Schuppenbildung: mit 60 Prozent der Fälle häufigstes Krankheitsbild, das vorwiegend Tiere mit intaktem Immunsystem entwickeln; beginnend am Kopf verbreitet sich die Erkrankung am gesamten restlichen Körper (sekundäre Sebadenitis;
- Hautgeschwüre über Knochenvorsprüngen, an Schwanzspitze und Ohren und im Haut-Schleimhaut-Übergang: betrifft 20 Prozent der befallenen Tiere und deutet auf eine geschwächte Immunabwehr hin. Die Symptome werden einerseits direkt durch die Parasiten hervorgerufen, können aber auch indirekt über eine von Immunkomplexen hervorgerufene Vaskulitis verursacht werden.
- Knötchenbildung in der Haut: In die Haut eingewanderte Makrophagen führen zur Ausbildung der Knötchen; weitere Abwehrzellen sind nur geringfügig beteiligt. Die Erkrankung tritt bei etwa 12 Prozent der Patienten auf und weist auf eine ungenügende Immunabwehr hin.
- generalisierte Hautdegeneration mit Pustelbildung im Bereich des Körperstammes: mit 4 Prozent die seltenste Form. Die Pusteln sind mit einer nichteitrigen Flüssigkeit und einigen Parasiten gefüllt. Die Pathogenese dieser Form ist nicht geklärt und es gibt keinen Hinweis auf einen Zusammenhang mit der Immunkompetenz des erkrankten Tieres.
- Re- oder intermittierendes Fieber mit zwei Spitzen pro Tag (doppelgipfliges Fieber) ist ein Hinweis auf eine viszerale Leishmaniose.
Neben den beschriebenen Störungen kann die Haut weitere Symptome wie übermäßige Verhornung, Krallenverkrümmung, Nagelbettentzündung und Pigmentverlust im Nasen-Maulbereich ausbilden. Auch die Schleimhäute können betroffen sein.
Neben der Erkrankung der Haut sind häufig gleichfalls die inneren Organe betroffen (viszerale Leishmaniose). Je nach Organbeteiligung ist die Ausbildung von Leberentzündungen, Darmentzündungen, Nierenversagen, Blutgefäßentzündungen, Knochenmarkentzündungen, Gelenkentzündungen, Nervenentzündungen und Muskelentzündungen möglich.
Infolge des sich ausgesprochen vielfältig darstellenden Krankheitsbildes kann die Diagnosefindung schwierig sein, zumal die Krankheit in den meisten Teilen Deutschlands nicht endemisch ist und daher oft nicht zur Routinediagnostik gehört.
Daneben gibt es keinen absolut zuverlässigen Test für die Krankheit.
Die Diagnosestellung beruht neben dem direkten Parasitennachweis vor allem auf Untersuchungen zur Immunantwort des Wirtes.
Therapie der viszeralen Leishmaniose
Häufig ist eine vollständige Heilung der Erkrankung nicht möglich. Die therapeutischen Ansätze konzentrieren sich daher neben der Erregerelimination vor allem auf eine Stärkung der körpereigenen zellulären Abwehr.
Übertragung
Die Übertragung erfolgt durch Sandmücken (aus der Familie der Schmetterlingsmücken). In den 1950er Jahren wurden durch den Einsatz von Insektiziden (hauptsächlich DDT) gegen Malaria-übertragende Anophelesmücken auch die Sandmücken (Phlebotominae) stark dezimiert. Heute haben sich die Sandmückenpopulationen wieder auf das ursprüngliche Niveau vermehrt, wodurch im Mittelmeerraum die Erkrankungszahlen an Leishmaniosen bei Mensch und Tier wieder zunehmen.
Die Leishmaniose-Infektionsrate von Hunden ist besonders im Mittelmeerraum stellenweise sehr hoch: In Andalusien sind bis zu 42 % der Hunde infiziert, auf Sizilien bis zu 80 %. Die Infektionsrate bei Menschen und Hunden hängt von der lokalen Sandmückenpopulation, deren Durchseuchung und Stechgewohnheiten ab.
Klinik, Diagnostik
Infolge der Tatsache, dass Leishmanien nahezu alle Organsysteme des Körpers befallen können, kann sich die Krankheit sehr vielfältig darstellen. Einem Großteil der erkrankten Tiere ist jedoch das Auftreten von Störungen der Haut gemein. Anhand der Verteilung dieser Störung können Rückschlüsse auf die Prognose der Erkrankung gezogen werden:
- symmetrischer Haarverlust und Schuppenbildung: mit 60 Prozent der Fälle häufigstes Krankheitsbild, das vorwiegend Tiere mit intaktem Immunsystem entwickeln; beginnend am Kopf verbreitet sich die Erkrankung am gesamten restlichen Körper (sekundäre Sebadenitis;
- Hautgeschwüre über Knochenvorsprüngen, an Schwanzspitze und Ohren und im Haut-Schleimhaut-Übergang: betrifft 20 Prozent der befallenen Tiere und deutet auf eine geschwächte Immunabwehr hin. Die Symptome werden einerseits direkt durch die Parasiten hervorgerufen, können aber auch indirekt über eine von Immunkomplexen hervorgerufene Vaskulitis verursacht werden.
- Knötchenbildung in der Haut: In die Haut eingewanderte Makrophagen führen zur Ausbildung der Knötchen; weitere Abwehrzellen sind nur geringfügig beteiligt. Die Erkrankung tritt bei etwa 12 Prozent der Patienten auf und weist auf eine ungenügende Immunabwehr hin.
- generalisierte Hautdegeneration mit Pustelbildung im Bereich des Körperstammes: mit 4 Prozent die seltenste Form. Die Pusteln sind mit einer nichteitrigen Flüssigkeit und einigen Parasiten gefüllt. Die Pathogenese dieser Form ist nicht geklärt und es gibt keinen Hinweis auf einen Zusammenhang mit der Immunkompetenz des erkrankten Tieres.
- Re- oder intermittierendes Fieber mit zwei Spitzen pro Tag (doppelgipfliges Fieber) ist ein Hinweis auf eine viszerale Leishmaniose.
Neben den beschriebenen Störungen kann die Haut weitere Symptome wie übermäßige Verhornung, Krallenverkrümmung, Nagelbettentzündung und Pigmentverlust im Nasen-Maulbereich ausbilden. Auch die Schleimhäute können betroffen sein.
Neben der Erkrankung der Haut sind häufig gleichfalls die inneren Organe betroffen (viszerale Leishmaniose). Je nach Organbeteiligung ist die Ausbildung von Leberentzündungen, Darmentzündungen, Nierenversagen, Blutgefäßentzündungen, Knochenmarkentzündungen, Gelenkentzündungen, Nervenentzündungen und Muskelentzündungen möglich.
Infolge des sich ausgesprochen vielfältig darstellenden Krankheitsbildes kann die Diagnosefindung schwierig sein, zumal die Krankheit in den meisten Teilen Deutschlands nicht endemisch ist und daher oft nicht zur Routinediagnostik gehört.
Daneben gibt es keinen absolut zuverlässigen Test für die Krankheit.
Die Diagnosestellung beruht neben dem direkten Parasitennachweis vor allem auf Untersuchungen zur Immunantwort des Wirtes.
Therapie der viszeralen Leishmaniose
Häufig ist eine vollständige Heilung der Erkrankung nicht möglich. Die therapeutischen Ansätze konzentrieren sich daher neben der Erregerelimination vor allem auf eine Stärkung der körpereigenen zellulären Abwehr.
eingestellt von: ise; Quellen- und Bildnachweis
x

Quellen- und Bildnachweis

Bildname:
Viszerale Leishmaniose mit starker Abmagerung
Urheber:
Wikipedia/Dantas-Torres F. (2008)
Link:
Neosporose
Die Neosporose ist eine durch den Einzeller Neospora caninum hervorgerufene Infektionskrankheit bei Haus- und Wildtieren. Sie tritt vor allem bei Hunden auf und kann bei diesen eine neurologische Erkrankung auslösen, die sich vor allem als Hirnstammsyndrom äußert.
Erreger
Hunde infizieren sich über die Aufnahme von rohen Tierprodukten (Gehirn, Fleisch). Im Darm der Hunde werden die Zysten bei der Verdauung freigesetzt und beginnen sich zu vermehren. Tachyzoiten kommen im Gehirn, Rückenmark, in der Bauchspeicheldrüse, Skelettmuskulatur, Haut, Leber und in den Lungen vor. Zysten, die nur aus Bradyzoiten entstehen, entwickeln sich nur im Nervengewebe.
Hunde sind in Europa häufig infiziert, allerdings ruft die Infektion nur selten eine Erkrankung hervor, sondern verläuft meist latent ohne klinische Erscheinungen.
Krankheitsbilder
Eine ernsthafte Erkrankung manifestiert sich vor allem als Meningoenzephalitis des Stammhirns mit Ausbildung eines Hirnstammsyndroms. Hierbei treten Lähmungen der hinteren Hirnnerven (vor allem Fazialislähmung), Ausfälle des oberen Motoneurons (Tremor, Ataxie, Parese) und Kopfschiefhaltungen auf.
Weitere Krankheitsbilder durch Neosporosa caninum beim Hund sind Polyneuritis, Polymyositis, Leberentzündungen (Hepatitis), Lungenentzündungen (Pneumonie) und geschwürige Dermatitiden.
Diagnostik
Im Hirnwasser-Punktat kann eine Pleozytose mit eosinophilen Granulozyten nachgewiesen werden.
Eine Bestimmung der Antikörper kann mittels Immunfluoreszenz oder ELISA erfolgen, ebenfalls ein direkter Erregernachweis über PCR im Kot. Diese Nachweise belegen allerdings nur eine Infektion, ein kausaler Zusammenhang zur beobachteten Erkrankung muss nicht bestehen.
Erreger
Hunde infizieren sich über die Aufnahme von rohen Tierprodukten (Gehirn, Fleisch). Im Darm der Hunde werden die Zysten bei der Verdauung freigesetzt und beginnen sich zu vermehren. Tachyzoiten kommen im Gehirn, Rückenmark, in der Bauchspeicheldrüse, Skelettmuskulatur, Haut, Leber und in den Lungen vor. Zysten, die nur aus Bradyzoiten entstehen, entwickeln sich nur im Nervengewebe.
Hunde sind in Europa häufig infiziert, allerdings ruft die Infektion nur selten eine Erkrankung hervor, sondern verläuft meist latent ohne klinische Erscheinungen.
Krankheitsbilder
Eine ernsthafte Erkrankung manifestiert sich vor allem als Meningoenzephalitis des Stammhirns mit Ausbildung eines Hirnstammsyndroms. Hierbei treten Lähmungen der hinteren Hirnnerven (vor allem Fazialislähmung), Ausfälle des oberen Motoneurons (Tremor, Ataxie, Parese) und Kopfschiefhaltungen auf.
Weitere Krankheitsbilder durch Neosporosa caninum beim Hund sind Polyneuritis, Polymyositis, Leberentzündungen (Hepatitis), Lungenentzündungen (Pneumonie) und geschwürige Dermatitiden.
Diagnostik
Im Hirnwasser-Punktat kann eine Pleozytose mit eosinophilen Granulozyten nachgewiesen werden.
Eine Bestimmung der Antikörper kann mittels Immunfluoreszenz oder ELISA erfolgen, ebenfalls ein direkter Erregernachweis über PCR im Kot. Diese Nachweise belegen allerdings nur eine Infektion, ein kausaler Zusammenhang zur beobachteten Erkrankung muss nicht bestehen.
eingestellt von: ise; Quellennachweis
Peitschenwurmbefall des Hundes
Peitschenwurmbefall des Hundes (Trichuriasis), die Infektion mit Peitschenwürmern, ist eine Parasitose bei Hunden, die im Allgemeinen zu mildem bis mittelgradigem Durchfall führt.
Die Erkrankung wird durch die mikroskopische Untersuchung einer Kotprobe auf Eier nachgewiesen.
Krankheitsbild
Befallene Hunde zeigen Durchfall, der blutig, bei weniger schwerem Verlauf mit Schleim durchsetzt ist. Stuhlzwang ist häufig. Die Tiere magern ab, Jungtiere bleiben im Wachstum zurück. Bei starkem Befall kann sich eine Typhlitis und Kolitis mit Bauchschmerzen, Erbrechen, Fressunlust, Austrocknung und Blutarmut entwickeln.
In Extremfällen kann es zu Entgleisung der Serumelektrolyte mit Hyponatriämie und Hyperkaliämie kommen. Eine sichere Diagnose kann nur über den Einachweis im Kot mittels Flotationsverfahren gestellt werden.
Die Erkrankung wird durch die mikroskopische Untersuchung einer Kotprobe auf Eier nachgewiesen.
Krankheitsbild
Befallene Hunde zeigen Durchfall, der blutig, bei weniger schwerem Verlauf mit Schleim durchsetzt ist. Stuhlzwang ist häufig. Die Tiere magern ab, Jungtiere bleiben im Wachstum zurück. Bei starkem Befall kann sich eine Typhlitis und Kolitis mit Bauchschmerzen, Erbrechen, Fressunlust, Austrocknung und Blutarmut entwickeln.
In Extremfällen kann es zu Entgleisung der Serumelektrolyte mit Hyponatriämie und Hyperkaliämie kommen. Eine sichere Diagnose kann nur über den Einachweis im Kot mittels Flotationsverfahren gestellt werden.
eingestellt von: ise; Quellen- und Bildnachweis
x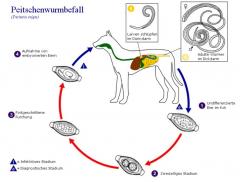

Quellen- und Bildnachweis

Bildname:
Peitschenwurmbefall des Hundes
Urheber:
Wikipedia/Anka Friedrich
Link:
Sarcoptes-Räude ( Fuchsräude ) des Hundes
Die Sarcoptes-Räude ( Fuchsräude ) des Hundes ist eine hochansteckende parasitäre Hauterkrankung die durch die Räudemilbe Sarcoptes scabiei var. canis hervorgerufen wird. Sie ist durch gerötete Papeln, bei schwerem Verlauf durch krustöse Hautveränderungen gekennzeichnet. Die Bekämpfung erfolgt durch milbenabtötende Mittel (Akarizide).
Vorkommen und Krankheitsentstehung
Die zu den Grabmilben gehörende Sarcoptes-Milbe des Hundes (Sarcoptes scabiei var. canis, gelegentlich auch als eigene Art Sarcoptes canis aufgefasst) ist ein vor allem bei Hunden vorkommender Parasit mit relativ hoher Wirtsspezifität. Gelegentlich kann er auch beim Rotfuchs und bei Hauskatzen auftreten. Selbst beim Menschen kann sie eine kurzzeitige Erkrankung mit Juckreiz und kleinen Papeln auslösen, heilt er aber im Regelfall spontan nach wenigen Tagen aus („Pseudo-Krätze“).
Der gesamte Entwicklungszyklus der Milbe findet auf beziehungsweise in der Haut des Hundes statt. Die Männchen leben auf der Hautoberfläche oder in flachen Tunneln. Dort findet die Kopulation statt, nach der sie absterben. Weibliche Grabmilben graben sich mit ihren Mundwerkzeugen (Chelizeren) in das Stratum spinosum oder granulosum der Epidermis ein und ernähren sich von Keratin und Gewebsflüssigkeit. Sie legen während ihres Lebens Eier in die von ihnen angelegten Bohrgänge. Der Entwicklungszyklus der Grabmilben dauert etwa 21 Tage und zeigt drei Entwicklungsstufen.
Aus den Eiern schlüpfen nach 3 bis 5 Tagen die Larven. Sie tragen nur drei Beinpaare und leben hauptsächlich in den Bohrgängen. Die Larven häuten sich in eigenen Hautnischen zu Nymphen, die morphologisch den adulten Weibchen ähneln, aber wesentlich kleiner und noch nicht geschlechtsdifferenziert sind. Diese häuten sich zu den adulten Grabmilben.
Die Übertragung erfolgt durch direkten Kontakt mit infizierten Tieren. Die Sarcoptes-Räude ist hochansteckend.
Klinisches Bild
Die Sarcoptes-Räude zeigt sich zunächst in Form von geröteten kleinen Papeln, eventuell auch Pusteln. Sie treten vor allem an Ellenbogen und Bauch auf. Im weiteren Verlauf zu einer starken Hautrötung (Erythema) und infolge des starken Juckreizes zu selbstzugefügten Hautveränderungen wie Haarausfall (Alopezie), Schuppung, Krusten und übermäßiger Verhornung (Hyperkeratose). Häufig sind die Außenseiten der Gliedmaßen und die Ränder der Ohrmuschel betroffen.
Es wird angenommen, dass das klinische Bild weniger durch die Schadwirkung der Milben, sondern auf allergische Reaktionen zurückzuführen ist.
Die Diagnose wird durch ein oberflächliches Hautgeschabsel gesichert. Alternativ können zwei bis vier Wochen nach der Ansteckung über eine Blutuntersuchung Sarcoptes-spezifische Antikörper nachgewiesen werden.
Bekämpfung
Zur Bekämpfung eignen sich Waschbehandlungen mit Amitraz sowie Ivermectin (cave MDR1-Defekt), Selamectin, Milbemycin oder Moxidectin.
Vorkommen und Krankheitsentstehung
Die zu den Grabmilben gehörende Sarcoptes-Milbe des Hundes (Sarcoptes scabiei var. canis, gelegentlich auch als eigene Art Sarcoptes canis aufgefasst) ist ein vor allem bei Hunden vorkommender Parasit mit relativ hoher Wirtsspezifität. Gelegentlich kann er auch beim Rotfuchs und bei Hauskatzen auftreten. Selbst beim Menschen kann sie eine kurzzeitige Erkrankung mit Juckreiz und kleinen Papeln auslösen, heilt er aber im Regelfall spontan nach wenigen Tagen aus („Pseudo-Krätze“).
Der gesamte Entwicklungszyklus der Milbe findet auf beziehungsweise in der Haut des Hundes statt. Die Männchen leben auf der Hautoberfläche oder in flachen Tunneln. Dort findet die Kopulation statt, nach der sie absterben. Weibliche Grabmilben graben sich mit ihren Mundwerkzeugen (Chelizeren) in das Stratum spinosum oder granulosum der Epidermis ein und ernähren sich von Keratin und Gewebsflüssigkeit. Sie legen während ihres Lebens Eier in die von ihnen angelegten Bohrgänge. Der Entwicklungszyklus der Grabmilben dauert etwa 21 Tage und zeigt drei Entwicklungsstufen.
Aus den Eiern schlüpfen nach 3 bis 5 Tagen die Larven. Sie tragen nur drei Beinpaare und leben hauptsächlich in den Bohrgängen. Die Larven häuten sich in eigenen Hautnischen zu Nymphen, die morphologisch den adulten Weibchen ähneln, aber wesentlich kleiner und noch nicht geschlechtsdifferenziert sind. Diese häuten sich zu den adulten Grabmilben.
Die Übertragung erfolgt durch direkten Kontakt mit infizierten Tieren. Die Sarcoptes-Räude ist hochansteckend.
Klinisches Bild
Die Sarcoptes-Räude zeigt sich zunächst in Form von geröteten kleinen Papeln, eventuell auch Pusteln. Sie treten vor allem an Ellenbogen und Bauch auf. Im weiteren Verlauf zu einer starken Hautrötung (Erythema) und infolge des starken Juckreizes zu selbstzugefügten Hautveränderungen wie Haarausfall (Alopezie), Schuppung, Krusten und übermäßiger Verhornung (Hyperkeratose). Häufig sind die Außenseiten der Gliedmaßen und die Ränder der Ohrmuschel betroffen.
Es wird angenommen, dass das klinische Bild weniger durch die Schadwirkung der Milben, sondern auf allergische Reaktionen zurückzuführen ist.
Die Diagnose wird durch ein oberflächliches Hautgeschabsel gesichert. Alternativ können zwei bis vier Wochen nach der Ansteckung über eine Blutuntersuchung Sarcoptes-spezifische Antikörper nachgewiesen werden.
Bekämpfung
Zur Bekämpfung eignen sich Waschbehandlungen mit Amitraz sowie Ivermectin (cave MDR1-Defekt), Selamectin, Milbemycin oder Moxidectin.
eingestellt von: ise; Quellen- und Bildnachweis
x

Quellen- und Bildnachweis

Bildname:
Hochgradige Sarcoptes-Räude bei einem verwilderten Straßenhund
Urheber:
Wikipedia/Jack Merridew
Link:
Neuen Eintrag erstellen  Einstieg in die Dooggs-Portal-Werbung | Basic-Paket!Sie suchen eine sehr günstige Möglichkeit im Dooggs-Portal zu werben?, Sie bieten Dienstleistungen zum Thema rund um den Hund an?, Dann ist unser Einsteiger-Werbe-Paket Basic
Einstieg in die Dooggs-Portal-Werbung | Basic-Paket!Sie suchen eine sehr günstige Möglichkeit im Dooggs-Portal zu werben?, Sie bieten Dienstleistungen zum Thema rund um den Hund an?, Dann ist unser Einsteiger-Werbe-Paket Basic Die mobile Trimmtante mit Herz!Das bin ich. Sarah Morich, geboren am 08.07.1991 in Herzberg am Harz. Seitdem ich mich erinnern kann, sind wir im Besitz von Hunden.2014 sagte ich mir.. warum, nicht Hobby zum Beruf gesagt, getan.. Ich machte mich selbständig als mobile
Die mobile Trimmtante mit Herz!Das bin ich. Sarah Morich, geboren am 08.07.1991 in Herzberg am Harz. Seitdem ich mich erinnern kann, sind wir im Besitz von Hunden.2014 sagte ich mir.. warum, nicht Hobby zum Beruf gesagt, getan.. Ich machte mich selbständig als mobile Physiotherapie Hund & Pferd | M. SteinTierheilpraxis M. Stein | DiagnostikUntersuchungNur eine umfassende Untersuchung kann zu einer erfolgreichen Therapie und somit zu einem gesunden Tier führen! RöntgendiagnostikWenn wir die Möglichkeiten haben
Physiotherapie Hund & Pferd | M. SteinTierheilpraxis M. Stein | DiagnostikUntersuchungNur eine umfassende Untersuchung kann zu einer erfolgreichen Therapie und somit zu einem gesunden Tier führen! RöntgendiagnostikWenn wir die Möglichkeiten haben Traumhund - Training für Mensch und Hund im Kreis SoestTraumhund - Hundetraining im Kreis Soest hilft Ihnen dabei, den für Sie beide passenden Weg zu finden:Traumhund-Hundetraining – Teamwork macht
Traumhund - Training für Mensch und Hund im Kreis SoestTraumhund - Hundetraining im Kreis Soest hilft Ihnen dabei, den für Sie beide passenden Weg zu finden:Traumhund-Hundetraining – Teamwork macht Z.O.P.F Hundeschule in Villingen-SchwenningenTraining ohne Leckerchen?!Ja, es ist möglich, sofern der Hund sich durch andere Dinge motivieren lässt. Das können Streicheleinheiten sein, einfach nur Nähe, Spielzeug oder Dinge, die der Hund grade lieber machen möchte.Manche
Z.O.P.F Hundeschule in Villingen-SchwenningenTraining ohne Leckerchen?!Ja, es ist möglich, sofern der Hund sich durch andere Dinge motivieren lässt. Das können Streicheleinheiten sein, einfach nur Nähe, Spielzeug oder Dinge, die der Hund grade lieber machen möchte.Manche „Mein Hund fürs Leben“ (ZDF)Die Redaktion der TV-Produktionsfirma „Tower Productions“ in Berlin, sucht aktuell für die zweite Staffel der Fernsehsendung „Mein Hund fürs Leben“ (ZDF) Menschen, die einen Hund aus dem Tierheim adoptieren möchten und sich auf diesem
„Mein Hund fürs Leben“ (ZDF)Die Redaktion der TV-Produktionsfirma „Tower Productions“ in Berlin, sucht aktuell für die zweite Staffel der Fernsehsendung „Mein Hund fürs Leben“ (ZDF) Menschen, die einen Hund aus dem Tierheim adoptieren möchten und sich auf diesem
DOOGGS NEWS
 Einstieg in die Dooggs-Portal-Werbung | Basic-Paket!Sie suchen eine sehr günstige Möglichkeit im Dooggs-Portal zu werben?, Sie bieten Dienstleistungen zum Thema rund um den Hund an?, Dann ist unser Einsteiger-Werbe-Paket Basic
Einstieg in die Dooggs-Portal-Werbung | Basic-Paket!Sie suchen eine sehr günstige Möglichkeit im Dooggs-Portal zu werben?, Sie bieten Dienstleistungen zum Thema rund um den Hund an?, Dann ist unser Einsteiger-Werbe-Paket Basic Die mobile Trimmtante mit Herz!Das bin ich. Sarah Morich, geboren am 08.07.1991 in Herzberg am Harz. Seitdem ich mich erinnern kann, sind wir im Besitz von Hunden.2014 sagte ich mir.. warum, nicht Hobby zum Beruf gesagt, getan.. Ich machte mich selbständig als mobile
Die mobile Trimmtante mit Herz!Das bin ich. Sarah Morich, geboren am 08.07.1991 in Herzberg am Harz. Seitdem ich mich erinnern kann, sind wir im Besitz von Hunden.2014 sagte ich mir.. warum, nicht Hobby zum Beruf gesagt, getan.. Ich machte mich selbständig als mobile Physiotherapie Hund & Pferd | M. SteinTierheilpraxis M. Stein | DiagnostikUntersuchungNur eine umfassende Untersuchung kann zu einer erfolgreichen Therapie und somit zu einem gesunden Tier führen! RöntgendiagnostikWenn wir die Möglichkeiten haben
Physiotherapie Hund & Pferd | M. SteinTierheilpraxis M. Stein | DiagnostikUntersuchungNur eine umfassende Untersuchung kann zu einer erfolgreichen Therapie und somit zu einem gesunden Tier führen! RöntgendiagnostikWenn wir die Möglichkeiten haben Traumhund - Training für Mensch und Hund im Kreis SoestTraumhund - Hundetraining im Kreis Soest hilft Ihnen dabei, den für Sie beide passenden Weg zu finden:Traumhund-Hundetraining – Teamwork macht
Traumhund - Training für Mensch und Hund im Kreis SoestTraumhund - Hundetraining im Kreis Soest hilft Ihnen dabei, den für Sie beide passenden Weg zu finden:Traumhund-Hundetraining – Teamwork macht Z.O.P.F Hundeschule in Villingen-SchwenningenTraining ohne Leckerchen?!Ja, es ist möglich, sofern der Hund sich durch andere Dinge motivieren lässt. Das können Streicheleinheiten sein, einfach nur Nähe, Spielzeug oder Dinge, die der Hund grade lieber machen möchte.Manche
Z.O.P.F Hundeschule in Villingen-SchwenningenTraining ohne Leckerchen?!Ja, es ist möglich, sofern der Hund sich durch andere Dinge motivieren lässt. Das können Streicheleinheiten sein, einfach nur Nähe, Spielzeug oder Dinge, die der Hund grade lieber machen möchte.Manche „Mein Hund fürs Leben“ (ZDF)Die Redaktion der TV-Produktionsfirma „Tower Productions“ in Berlin, sucht aktuell für die zweite Staffel der Fernsehsendung „Mein Hund fürs Leben“ (ZDF) Menschen, die einen Hund aus dem Tierheim adoptieren möchten und sich auf diesem
„Mein Hund fürs Leben“ (ZDF)Die Redaktion der TV-Produktionsfirma „Tower Productions“ in Berlin, sucht aktuell für die zweite Staffel der Fernsehsendung „Mein Hund fürs Leben“ (ZDF) Menschen, die einen Hund aus dem Tierheim adoptieren möchten und sich auf diesem